En ny model for aktivering af immunsystemet
Ved at studere et stort protein (C1 proteinet) med røntgenstråling og elektronmikroskopi har forskere fra Aarhus Universitet gjort op med en gammel model for, hvorledes en vigtig del det medfødte immunforsvar aktiveres. Aktivering af C1 proteinet er en yderst vigtig mekanisme inden for immunologien, hvorfor de nye forskningsresultater også har et medicinsk potentiale.
En vigtig brik i immunforsvaret er det såkaldte komplementsystem. Når immunsystemet opdager en mikroorganisme eller andre tegn på fare, omdannes komplementproteinet C1 til et aktivt enzym, som kan kløve andre proteiner og dermed igangsætte en kædereaktion. Slutresultatet af dette bliver, at f.eks. invaderende patogene mikroorganismer optages af vores immunceller, og der startes en betændelsesreaktion, som leder til drab af mikroorganismerne. Inden for de seneste år er der kommet ekstra fokus på C1 proteinet, idet det ud over sin funktion i immunsystemet har vist sig at være dybt involveret i udviklingen af vores nervesystem og neurologiske sygdomme.
Lærebøger i immunologi siger, at C1 proteinet aktiveres ved, at der sker en meget kompliceret ændring i strukturen internt i det enkelte C1 molekyle, når det genkender f.eks. en patogen organisme. De nye forskningsresultater fra Aarhus Universitet gør op med dette dogme og viser, at aktivering af komplementsystemet sker mellem to C1 proteiner, når de kommer tæt nok på hinanden, hvilket er en meget mere simpel og generel mekanisme.
Tæt samarbejde førte til resultaterne
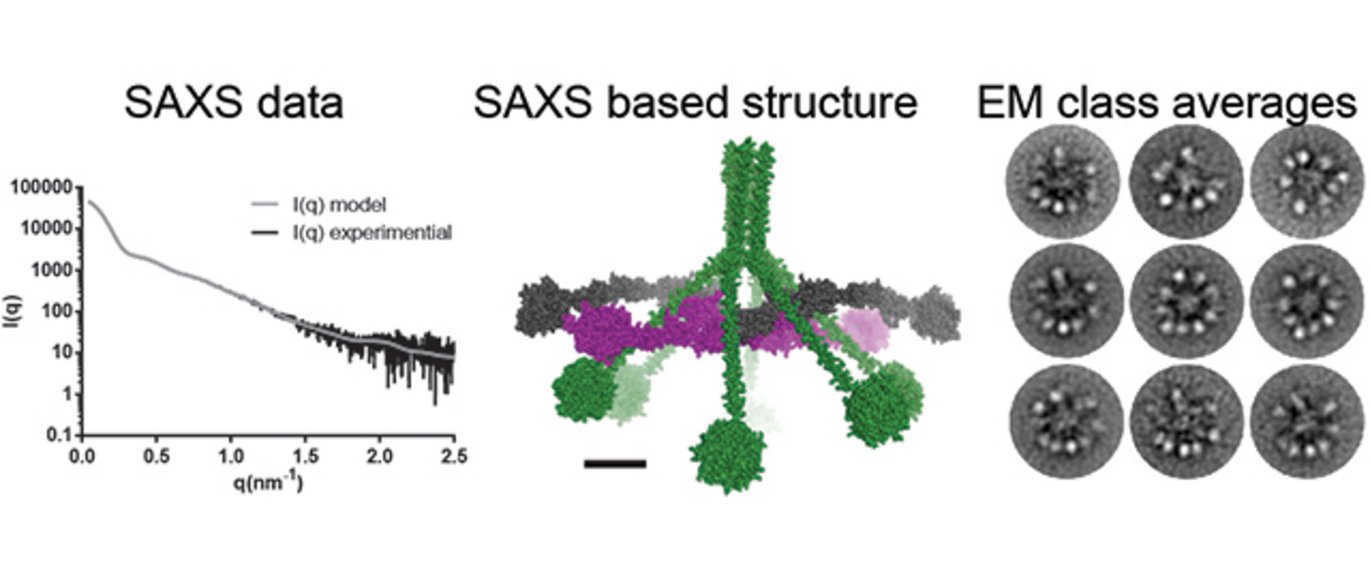
De nye resultater er skabt gennem et tæt samarbejde mellem fire forskningsgrupper på Aarhus Universitet. Postdoc Simon A. Mortensen isolerede først en speciel version af C1 komplekset sammen med professor Steffen Thiel fra Institut for Biomedicin. Også professor Jens Christian Jensenius og laborant Annette Hansen deltog i dette arbejde. Disse prøver blev analyseret i samarbejde med lektor Bjørn Sander og lektor Monika Golas på Biomedicin med elektronmikroskopi, hvor enkelte C1 molekyler kunne identificeres.
”Jeg havde omhyggeligt optimeret min protokol til fremstilling af C1 komplekset, og det tog lang tid, altså mindst et år, at få lavet den helt rigtige prøve,” udtaler Simon A. Mortensen. ”Men den første gang jeg så C1 molekylet tydeligt sammen med Bjørn og Monika, var jeg helt oppe at køre, og det var bestemt alt sliddet værd.”
Parallelt med dette brugte ph.d.-studerende Rasmus K. Jensen røntgenstråling til at undersøge strukturen af Simons C1 protein i opløsning under vejledning af professor Gregers Rom Andersen fra Institut for Molekylærbiologi og Genetik med assistance af professor Jan Skov Pedersen fra iNANO centeret. Jan og Simon lavede de første målinger i Aarhus med røntgenstråling, mens Simon, Rasmus og Gregers indsamlede de bedste data på PETRA III synktronen i Hamburg, og Rasmus brugte derefter måneder på at analysere disse data.
”C1 komplekset var egentligt for stort og kompliceret til, at vores computerprogrammer kunne beregne dets struktur”, fortæller Rasmus K. Jensen. ”Så jeg fik lavet en speciel version til formålet. Derefter måtte jeg gennem mange cykler af beregninger, som hver tog 14 dage, på trods af at jeg anvender kraftige computere.”
”C1 komplekset er det største og mest komplicerede protein, jeg har arbejdet med i snart 30 år. Dets struktur er også meget usædvanlig, så det har været udfordrende men også virkeligt interessant,” supplerer professor Gregers Rom Andersen.
Resultaterne viste, at den gamle model for aktivering af C1 proteinet måtte skrottes, da den simpelthen var fysisk umulig.
”Vi har gennem de sidste fire-fem år haft på fornemmelsen, at den gamle model ikke kunne være rigtig,” udtaler professor Steffen Thiel. ”Derudover har vi for tre år siden vist, at et tilsvarende protein, som har en lignende funktion i en anden gren af komplementsystemet, aktiveres på samme måde. De nye resultater for C1 proteinet gør derfor, at vi kan foreslå en helt generel model for aktivering af komplement. Dermed har vi nu en bedre forståelse for, hvorledes vores immunsystem fungerer,” slutter Steffen Thiel.
Forskningen er blevet offentliggjort i det anerkendte tidsskrift Proceedings of the National Academy of Sciences USA (PNAS).
Mere information
Professor Gregers Rom Andersen
Institut for Molekylærbiologi og Genetik
Aarhus Universitet
gra@mbg.au.dk - 3025 6646
Professor Steffen Thiel
Institut for Biomedicin
Aarhus Universitet
st@biomed.au.dk - 2927 0890
