Forskere studerer blodets hemmeligheder
Man har længe kendt til de faktorer, som styrer blodets koagulation. Ny forskning viser, at den sidste faktor – Faktor XIII, som stabiliserer sårdannelsen – spiller en langt mere kompliceret rolle end hidtil troet.

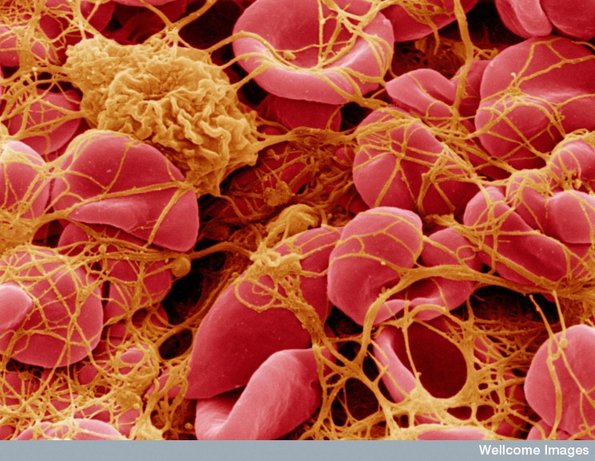
En af kroppens vigtigste forsvarsmekanismer er, at hvis der går hul på den, kan den få noget af blodet til at klumpe sig sammen i hullet og størkne, og dermed forhindre yderligere blodtab. Koagulationen er så at sige naturens eget plaster.
Plasteret skal imidlertid både være holdbart og let at nedbryde.
Når vi f.eks. skærer os i fingeren, skal plasteret – altså blodklumpen og i sidste ende sårskorpen - helst dannes hurtigt og være så solid, at blødningen ikke begynder igen, før vævet nedenunder er helet.
Men hvis der går hul på væv eller blodkar inde i kroppen – som f.eks. ved en forstuvning eller et blåt mærke - skal blodklumperne kunne nedbrydes igen hurtigt, så de ikke danner blodpropper.
Livsvigtig balance
Kroppens forsvar mod læsioner skal med andre ord være nøje afbalanceret, så det stopper blødning effektivt, uden at det bliver alt for effektivt – og ikke forsøge at stoppe blødninger, der ikke er der.
Hos mange mennesker er mekanismen ude af balance. Nogles blod koagulerer lidt for ivrigt, eller deres system til at nedbryde blodklumperne fungerer ikke godt nok - blodpropper er en af de hyppigste dødsårsager i verden – mens andre har det modsatte problem: deres blod har svært ved at koagulere.
Alene i Danmark er ca. 1000 mennesker diagnosticeret med en blødersygdom, men det menes at langt flere har den mest almindelige af slagsen, von Willebrandts sygdom, uden at vide det.
Derfor forskes der over hele verden i de mange forskellige faktorer og processer, som indgår i koagulationen.
Analyse af blod
Således også på Institut for Molekylær Biologi og Genetik (MBG) på Aarhus Universitet. Her har et forskerhold brugt topmoderne udstyr til separation, proteinanalyse og massespektroskopi af blod, og analyseret hvilken rolle, den afsluttende faktor i koagulationen spiller.
Den kaldes Faktor XIII, og resultaterne fra Aarhus viser, at Faktor XIII er langt mere alsidig, end man er gået ud fra, siden den blev navngivet i 1963.
Meget tyder således på, at den bl.a. spiller sammen med kroppens øvrige immunsystem og dannelsen af bindevæv.
Resultaterne er publiceret i det amerikanske tidsskrift Journal of Biological Chemistry, og vi vender tilbage til dem senere. Først lidt om koagulationsfaktorernes orden:
Faktorerne flyder
Når vores væv eller blodkar beskadiges, sætter det gang i de såkaldte koagulationsfaktorer.
Disse faktorer består af blodplasma-proteiner, som kan aktiveres til at fungere som enzymer, der dels har hver deres opgave, dels understøtter hinandens funktioner. Faktorerne er traditionelt blevet nummereret med romertal, så de første 11 faktorer kaldes Faktor I – XIII (ja, der mangler ganske rigtigt to; den fjerde kaldes nemlig ikke længere Faktor IV, fordi den består af kalcium-ioner og ikke protein, og nummer VI viste sig at være en aktiveret Faktor V).
Under normale forhold er faktorerne inaktive, mens de cirkulerer rundt i blodbanen. Men i det øjeblik der går hul på et blodkar vil de nærmeste blodplader binde sig til kollagenet i bindevævet, samtidig med at et andet protein i bindevævet virker som en receptor for de næste forbipasserende Faktor VII-proteiner.
Kaskade af reaktioner
Når en handling sætter gang i flere reaktioner, som hver især sætter gang i nye reaktioner osv. – omtrent som væltende dominobrikker – kaldes det en kaskadereaktion.
Og her er der virkelig tale om en kaskadereaktion. Vi nøjes med en kort gennemgang:
Så snart Faktor VII har parkeret ved såret bliver den aktiveret og begynder at aktivere forbipasserende Faktor X proteiner, som derefter – med hjælp fra Faktor V – omdanner Faktor II til enzymet thrombin, som igen omdanner forbipasserende Faktor I, V, VII, VIII, XI og XIII til deres aktive former.
Thrombinet aktiverer samtidig de blodplader, som danner det første skrøbelige plaster på hullet, så deres overflade ændres fra glat til noget, der ligner velcro, som både kan holde fast og tiltrække andre koagulationsfaktorer.
Men det interessante i denne sammenhæng er aktiveringen af Faktor I og XIII. Faktor I omdannes til fibrin, og aktivt Faktor XIII til et enzym som stabiliserer fibrin.
Fibrin er proteiner, som samler sig i kæder og danner uopløselige fibre, der tætner og stabiliserer proppen af blodplader. Faktor XIII sætter så at sige kronen på værket ved danne krydsbindinger mellem fibrin-fibrene, så de ikke rives løs, men virker som et net, der holder sammen på klumpen af koaguleret blod.
Ned med nettet
Straks efter at fibrindannelsen er begyndt, starter en modsatrettet proces, fibrinolyse, som går ud på at opløse blodklumpen igen. Her spiller enzymet plasmin en vigtig rolle, idet plasmin nedbryder fibrin-fibrene.
”Imidlertid forsyner Faktor XIII fibrene med nogle andre proteiner, som hæmmer fibrinolysen. Det er praktisk, når det drejer sig om f.eks. snitsår i fingeren, for da har vi brug for en stabil sårskorpe, ind til vævshelingen er godt i gang. Men hvis fibrinet nedbrydes for hurtigt, begynder såret at bløde igen,” fortæller Camilla Lund Nikolajsen, som er ph.d.-studerende på MBG og førsteforfatter på den videnskabelige artikel.
Det ser man netop hos personer med den yderst sjældne blødersygdom, der skyldes manglende Faktor XIII: de kan godt danne blodklumper, men ikke ret længe ad gangen, så begynder de at bløde igen. Novo Nordisk sendte i 2013 en forebyggende behandling på markedet, bestående af rekombinant aktiveret Faktor XIII.
Men som oven for nævnt er det ikke hensigtsmæssigt at hæmme fibrinolysen, hvis koagulationen finder sted inde i kroppen og danner blodpropper. Desværre skelner Faktor XIII ikke mellem de to situationer.
Der er altså indlysende grunde til at se nærmere på Faktor XIII.
Faktor XIII kan meget mere -
De nye resultater fra Aarhus rejser imidlertid nye spørgsmål.
Forskningsprojektet gik ud på at kortlægge, hvilke proteiner der påvirkes af (fungerer som substrater for) enzymet Faktor XIII – et felt, som MBG i forvejen har bidraget til.
Hidtil har man kendt til 20 sådanne substrater i blodet. Den nye undersøgelse afslørede yderligere 132, som aldrig tidligere er blevet beskrevet.
Dermed er vi nu oppe på i alt 152proteiner - men kun 48 af dem blev inkorporeret i fibrin under koagulationsprocessen; de 99 andre ser umiddelbart ikke ud til at have noget at gøre med koagulation. Ikke direkte, i hvert fald.
– men hvad og hvordan?
”Vi har fundet ud af, at Faktor XIII har en langt bredere funktion end blot at stabilisere fibrin. Vi ved, at disse identificerede substrater har funktioner i henholdsvis koagulationssystemet, immunsystemet, i det inflammatoriske system og i dannelsen af bindevæv. Det ser ud som om koaguleringsprocessen og immunforsvaret vekselvirker, så Faktor XIII tager nogle proteiner fra immunsystemet og fikserer dem i sårskorpen ved hjælp af de krydsbindinger, som Faktor XIII laver. Men vi ved endnu ikke hvorfor,” forklarer Camilla Lund Nikolajsen.
Hun understreger, at de nye resultater ikke sig selv giver nøglen til at forhindre blodpropper eller bedre blødermedicin.
”Vores resultater kan guide fremtidig forskning indenfor koagulationsfeltet, så man får en bedre forståelse af Faktor XIII’s rolle i koagulation. Det kan på længere sigt føre til en bedre behandling af Faktor XIII-mangel og ikke mindst en bedre medicinsk behandling af blodpropper,” siger hun.
Link til den videnskabelige artikel i det amerikanske tidsskrift Journal of Biological Chemistry:
Coagulation Factor XIIIa Substrates in Human Plasma. Identification and Incorporation Into the Clot
Kontakt
Ph.d.-studerende Camilla Lund Nikolajsen
Institut for Molekyærbiologi og Genetik/iNANO
Aarhus Unversitet
email: camillan@mb.au.dk
87154932
