Hvordan bestemmes retningen for menneskets gener?
Et internationalt forskerhold anført af forskere fra Aarhus Universitet har fundet en mekanisme, der afgør, at tusindvis af ikke-kodende RNA-molekyler hurtigt forsvinder fra celler, mens de molekyler, der indeholder koder til protein-produktion, bliver bevaret. Resultaterne er med til at give en større forståelse for mekanismerne i det humane genom.
Som i alle højerestående organismer er menneskets genetiske arvemasse lagret i DNA-molekyler bestående af ca. 3 milliarder byggestene, der tilsammen udgør "livets kode". Aflæsningen af denne information sker ved en proces kaldet "transskription", hvor et stort enzymkompleks (RNA polymerase II eller blot RNAPII) kopierer visse dele af DNAet til RNA, der efterfølgende bruges til at udføre vigtige funktioner i cellen. En af disse er produktionen af proteiner, som udgør en stor del af cellens byggestene og enzymer.
Når RNAPII skal kopiere DNA, leder det efter bestemte DNA-sekvenser, der fortæller, hvor transskriptionen skal begynde. Disse sekvenser, kaldet "gen-promotorer", dirigerer som regel også RNAPII i den retning - højre eller venstre - som enzymet skal bevæge sig på DNA-strengen. Således havde man så godt som altid fundet transskripter produceret fra én bestemt side af hver enkelt gen-promotor.
To-sidet aktivitet af aktive gen-promotorer
I 2008 opdagede forskere fra Center for mRNP Biogenese og Metabolisme, at der generelt findes transskriptionsaktivitet på begge sider af aktive gen-promotorer.
Transskripterne fra "den anden side" (så kaldte PROMoter uPstream Transcripts (PROMPTs)) var aldrig blevet opdaget før, fordi de er særdeles ustabile, og derfor havde undsluppet forskernes opmærksomhed. ’Tricket’, der blev brugt til at finde disse hidtil ukendte transskripter, var derfor at stabilisere dem ved at inaktivere det enzymkompleks, der normalt sørger for deres nedbrydning.
Transskription af PROMPTs kræver blot tilstedeværelsen af en gen-promoter, og PROMPT produktion er således koblet til produktionen af det protein-kodende RNA. Funktionen af PROMPTs er stadig ukendt, men hvad enten PROMPTs oprindeligt er et biprodukt af det "normale" gen-udtryk eller ej, så har evolutionen formentlig fundet en måde, hvorpå dette biologiske fænomen kan udnyttes. Ydermere pegede resultaterne på, at måden hvorpå vi hidtil havde forstået cellens gen-regulering skulle nytænkes. Og dette gav forskerne sig i kast med.
Promotorers to-sidede aktivitet holdes en-sidet vha. kontrolleret RNA-nedbrydning
Nu har forskerne så fundet svaret på, hvorfor PROMPTs hurtigt forsvinder fra celler, mens de tilstødende mRNAer bliver bevaret som funktionelle (protein-kodende) enheder.
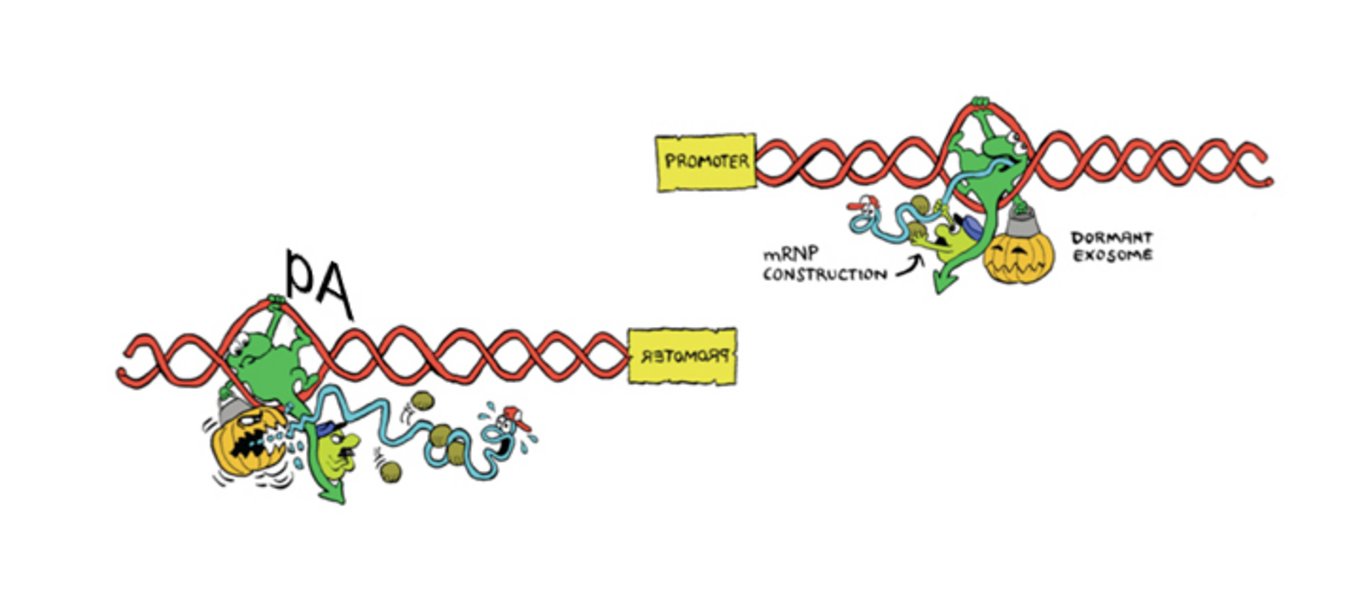
Det viser sig, at PROMPTs afsluttes på en måde, der til forveksling ligner den måde, hvorpå mRNAer afsluttes, dvs. ved hjælp af såkaldte polyadenylering (poly(A))-lignende signaler. Men en væsentlig forskel er dog, at opstrøms-antisense PROMPT 3'enderne - og dermed deres poly (A)-signaler - er koncentreret inden for en snæver afstand fra deres startsted. Dette gør de resulterende transskripter ekstremt ustabile.
Eftersom sådanne promoter-proksimale poly (A)-signaler er kraftigt nedprioriterede af evolutionen i 'mRNA retningen’ af gen-transskriptionen, kan en sådan asymmetrisk sekvensfordeling omkring gen-promotorer forklare, hvorledes RNA output bliver retningsbestemt fra en ellers to-sidet transskriptionsproces.
De nye forskningsresultater er netop offentliggjort online i tidsskriftet Nature Structural and Molecular Biology.
Forskerne vil nu forsøge at finde ud af, om den beskrevne mekanisme også bruges andre steder i det humane genom. Dette er et vigtigt spørgsmål, idet >90% af det humane genom bliver transskriberet, og cellen er nødt til at kontrollere et så massivt RNA output til kun at tillade funktionelle transskripters overlevelse.
Arbejdet blev udført af postdoc Evgenia Ntini og andre medlemmer af Torben Heick Jensens gruppe ved Danmark Grundsforskningsfonds Center for mRNP Biogenese og Metabolisme, Institut Molekylærbiologi og Genetik, Aarhus Universitet, i samarbejde med Lars Steinmetz’ gruppe ved EMBL i Heidelberg og Albin Sandelins gruppe ved BRIC i København.
Mere information
Professor Torben Heick Jensen
Institut for Molekylærbiologi og Genetik
Center for mRNP Biogenese og Metabolisme
Aarhus Universitet
thj@mb.au.dk - 6020 2705
