Hvordan taber et firben halen?
Dette spørgsmål har forskere fra Aarhus Universitet nu under stor international opmærksomhed fundet svaret på.

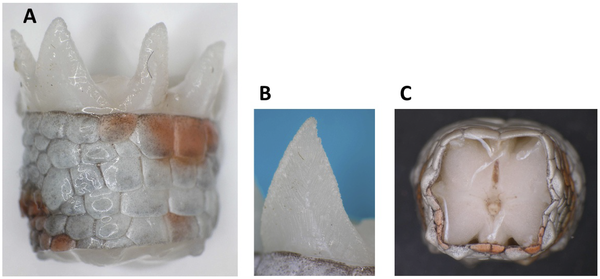
Når et firben føler sig truet af et rovdyr kan den med vilje tabe sin hale. Da halen bevarer evnen til at bevæge sig op til en halv time efter separationen, håber firbenet, at rovdyret angriber den tabte hale, så det i mellemtiden kan undslippe.
Denne evne har dog også visse ulemper, da halen bl.a. bruges som en fedtreserve. Derfor er det en fordel for firbenet, at det kan nøjes med at skille sig af med kun en mindre del af halen. Denne selvamputering (kaldet autotomi) af halen følger et bestemt mønster, da halen har foruddannede brudlinjer. Disse brudlinjer har forskerne nu beskrevet i en detaljegrad, der gør det muligt at forklare selvamputationsmekanismen.
Man håber, at denne opdagelse kan inspirere materialeforskere og ingeniører i deres design af nye materialer, hvor hurtig adskillelse er vigtig.
Studier i selvamputering
I projektet undersøgte man, hvad der gør et firben i stand til at tabe halen. Det viste sig, at halen har foruddannede brudlinjer, og strukturen af disse linjer blev i projektet karakteriseret med moderne former for biologisk visualiseringsudstyr.
Egentlig var det et tilfælde, at forskerne nåede frem til denne opdagelse. I forskergruppen, der ledes af professor Jan J. Enghild ved Aarhus Universitet, interesserer man sig bl.a. for at identificere nye proteolytiske enzymer (enzymer som kløver andre proteiner). Udover en grundlæggende fascination af selvamputering, så var det interessen for at identificere nye enzymer, som startede projektet, der nu er blevet publiceret.
-”Vi forestillede os, at proteolytiske enzymer måtte være involverede i processen, dels fordi vi regnede med, der ville ske en nedbrydning af væv, og dels fordi det normalt er protelytiske enzymer, der foretager en sådan nedbrydning. Hvis dette var tilfældet måtte det være utroligt effektive og aggressive enzymer, som kunne være meget interessante at kigge nærmere på, da disse potentielt kan bruges i industrien,” udtaler Jan J. Enghild.
I forbindelse med undersøgelsen brugte gruppen en moderne metode (proteomics) til at identificere proteiner – og dermed også enzymer – i komplekse blandinger. Denne undersøgelse viste, at proteolytiske enzymer ikke er involverede i selvamputering.
Foruddannede brudflader identificeres
Den nye opdagelse motiverede forskerne til at se nærmere på brudfladerne i firbenet. Man allierede sig derfor med kollegaer fra både biologi, medicin og kemi ved Aarhus Universitet, der analyserede brudfladerne med traditionelle vævssnit-analysemetoder, samt moderne metoder som scanning electron microscopy (SEM) og magnetic resonance imaging (MRI), som var til rådighed i den meget tværfaglige projektgruppe.
Efter at have indsamlet og sammenlignet resultaterne fra de forskellige metoder stod det efterhånden mere og mere klart for projektgruppen, at selvamputering er en mere mekanisk end biokemisk begivenhed. Med en bestemt afstand er der igennem hele firbenets hale foruddannede brudflader, og de nye data indikerer, at muskelfibrenes struktur i brudfladen ændrer sig i forbindelse med selvamputering, hvorved interaktionen imellem brudfladerne svækkes og selvamputeringen kan finde sted.
Det er mange år siden, at et grundigt studium af selvamputering er blevet lavet, og dengang havde man ikke de moderne redskaber til rådighed, som er blevet brugt i dette studium.
-”Det er de nye metoder og den tværfaglige tilgang til problemstillingen, som har gjort det muligt for os at komme et spadestik dybere i forståelsen af selvamputering,” udtaler Kristian W. Sanggaard fra projektgruppen.
Artiklen er publiceret i PLOS ONE. Her findes også en illustrativ 3D-film af halen baseret på MRI-resultaterne.
Yderligere information
Kristian Wejse Sanggaard
Institut for Molekylærbiologi og Genetik og
Interdisciplinært Nanoscience Center (iNANO)
Aarhus Universitet
krs@mb.au.dk; 2374 1497
