Norsk–dansk samarbejde afdækker protonkanal i bakterielt enzym
Et videnskabeligt samarbejde mellem forskere fra Oslo Universitet og Aarhus Universitet har afsløret en uventet kanal for fjernelse af protoner i krystalstrukturen af enzymet isatin hydrolase.


Isatin hydrolase, der et involveret i nedbrydningen af plantehormonet indol-3-eddikesyre, er identificeret i mange forskellige slags bakterier isoleret fra jord, vand, planter og menneskets tarm. Den første identifikation skete med jordbakterien Bradyrhizobium japonicum, som danner nitrogenfikserende rodknolde på værtsplanten sojabønne. Da den marine bakterie Labrenzia aggregata viste sig at have to gener, der koder for isatin hydrolase, valgte forskerne at studere enzymerne fra denne organisme nærmere.
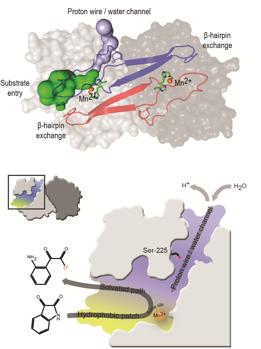
Det lykkedes ph.d.-studerende Kaare Bjerregaard-Andersen at opnå krystaller af de to isatin hydrolaser og at bestemme den tredimensionale struktur. Proteinet, som er en dimér, udviser en ny foldningsstruktur for et metalafhængigt (her Mn++) hydrolytisk enzym, hvor de to subunits udviser overlappende domæner. Mere interessant er identifikationen af to indgange til det aktive site, en kombineret vand- og protonkanal og en substrat- og produktkanal, som vist på figuren. Stærkt medvirkende til denne identifikation af vand- og protonkanalen har været krystaller, hvor en analog (thioisatin) af produktet er fanget i det aktive site. Isatin hydrolasen udviser et pH optimum på 9, hvorfor bortfjernelse af protoner, der dannes ved reaktionen, er påkrævet.
Ud over at isatin er et mellemprodukt i nedbrydningen af indol-3-eddikesyre, forefindes isatin i lave koncentrationer i blodet hos os mennesker og må formodes at være et nedbrydningsprodukt af neurotransmittere. Undersøgelser har vist, at niveauet af isatin er forhøjet i patienter med stress, og hos patienter der lider af Parkinsons sygdom. Det norsk-danske forskerhold har udført indledende forsøg med anvendelse af isatin hydrolase i en simpel enzymatisk screeningstest til bestemmelse af isatin i blod og urin.
Kaare Bjerregaard-Andersen er den første danske studerende, som opnår en dobbelt ph.d.-grad, som led i en aftale mellem Oslo Universitet og Aarhus Universitet. Kaare forsvarer sin ph.d.-afhandling i dag d. 30. juni 2014 i Oslo.
Link til artiklen i Journal of Biological Chemistry: A proton wire and water channel revealed in the crystal structure of isatin hydrolase
Mere information
Lektor Bjarne Jochimsen
Institut for Molekylærbiologi og Genetik
Aarhus Universitet
bjoc@mb.au.dk - 20275983
