Ny indsigt i et centralt biologisk dogme om iontransport
Nye forskningsresultater fra Aarhus Universitet og New York University viser, hvordan aktiv transport af kalium kan medieres gennem et membranproteinkompleks, der har rødder i både ionpumpe- og ionkanal-superfamilier. Resultaterne, der netop er publiceret i <em>Nature</em>, kaster nyt lys over, hvad der definerer kanaler og pumper i cellen.
Kalium er den primære ion i alle levende celler, og er afgørende for det såkaldte turgortryk. Hvis der er for meget kalium, kan cellen briste på grund af vandtilstrømning, hvis der er for lidt, vil cellen skrumpe. Dette osmotiske princip anvendes også i forbindelse med konservering af fødevarer, når der saltes eller tørres kød, frugt og grøntsager.
Da kalium ikke kan trænge gennem cellemembranen, har alle celler transportproteiner, der formidler kaliumoptaget. I encellede organismer er mekanismerne til at opretholde interne kaliumniveauer meget sensitive på grund af de udfordringer, som koncentrationssvingninger af kalium i vækstmiljøet medfører. Kaliumkanaler vil normalt skabe en indadgående strøm af kalium drevet af en elektrokemisk gradient. I miljøer med meget lav tilstedeværelse af kalium kan denne gradient imidlertid ikke opretholde interne kaliumniveauer, og en transport gennem kaliumpumpesystemer overtager hurtigt og sørger for et aktiv optag af kalium drevet direkte af kemisk energi.
Man forstår ikke disse kaliumpumpesystemers mekanisme og struktur særlig godt, men fra sekvensanalyse har man udledt, at de har elementer, der stammer fra både kaliumkanaler og mere klassiske natrium-/kaliumpumper, der er kendt fra dyr. Denne sammenblanding af kanal og pumpe har undret forskere i årtier, og mange har næsten tvivlet på eksistensen af disse komplekser som en funktionel enhed.
Dette skyldes til dels, at ideen om ”kanaler versus pumper” er et af de basale biologiske koncepter om iontransport, man lærer. Ionkanaler er kendt for at formidle hurtig og passiv transport med en elektrokemisk gradient, mens ionpumper er kendt for at formidle en langsom og aktiv transport mod en elektrokemisk gradient. Begge processer er velstuderede, og bliver normalt modstillede som fundamentalt forskellige.
Kanal- og pumpe-superfamilier skaber aktiv transport af kalium sammen
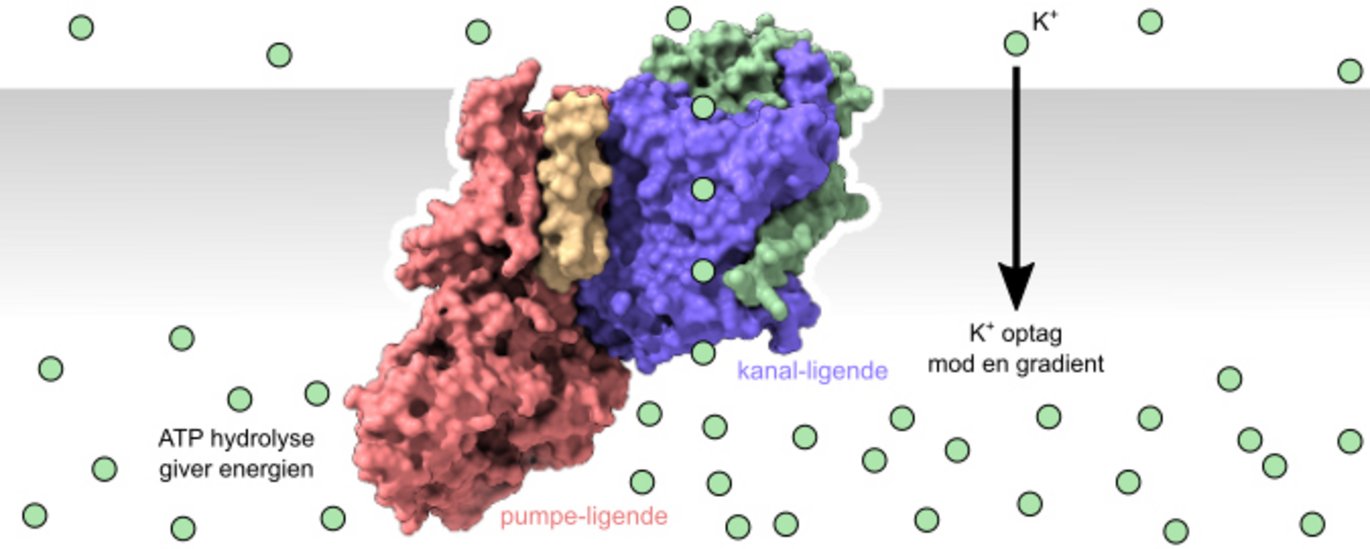
Nye resultater, der netop er offentliggjort i tidsskriftet Nature, udfordrer denne komfortable opdeling og forsøger at give svaret på, hvordan pumper og kanaler kan arbejde sammen i et kompleks. Det dansk-amerikanske forskerhold har for første gang visualiseret et kaliumtransportsystem, hvor medlemmer fra både kanal- og pumpe-superfamilier sammen danner et stort kompleks, hvor der skabes aktiv transport af kalium. Her sker der det, at den ”pumpelignende” del af komplekset genererer den energi (ligesom en motor), der driver den ”kanallignende” del af komplekset til at sørge for transport af kalium mod en 10.000-fold gradient af kalium.
"For mig er den mest fascinerende del af resultaterne, at de bryder med de kasser, som vi normalt forsøger at placere vores biologiske begreber i," siger AIAS-forsker og adjunkt Bjørn Panyella Pedersen, der er en del af holdet bag de nye resultater. "Det er endnu et fascinerende eksempel på, at naturen ser stort på vores forsøg på at klassificere den. Hvis evolution kan få noget til at ske, så sker det."
Resultaterne bygger oven på et stærkt fundament af grundlæggende viden om kanaler og pumper. Kanaler med kontrollerede åbne-/lukkemekanismer (porte) har været kendt og studeret i lang tid, og de fleste ionkanaler har faktisk en eller flere porte som en væsentlig del af deres fysiologiske funktion. Tilsvarende er den molekylære mekanisme bag ionpumper velstuderet. Med de nye resultater kan man pludselig se, hvordan porte på et ”kanallignende” subkompleks kan kobles op til et ”pumpelignende” subkompleks, der styrer portene. Derved skabes en stærk kobling mellem portåbning/-lukning, substratgenkendelse/-binding og energiforbrug. Disse elementer er alle kendetegn for aktiv transport kendt fra andre pumpesystemer, men her fungerer de kun, hvis alle elementer i komplekset er samlet.
"Dette har været et af de sværeste, men også mest fascinerende projekter, jeg har haft fornøjelsen af at arbejde på. Der er kommet så mange nye ideer ud af dette, og fortolkningen af resultaterne var udfordrende, da der virkelig skulle tænkes uden for boksen," siger Bjørn med et smil, inden han fortsætter, "David [Prof. David Stokes] var nøglen til dette, da han har arbejdet på komplekset i mange år og har en omfattende viden om systemets indretning. Dette har været en ægte teamindsats, og på baggrund af de ideer vi har nu, vil vi fortsætte vores samarbejde for at komme til at forstå, hvordan komplekset fungerer."
Resultaterne er offentliggjort i det prestigefyldte tidsskrift Nature.
Mere information
Adjunkt og AIAS fellow Bjørn Panyella Pedersen
Institut for Molekylærbiologi og Genetik og
Aarhus Institute of Advanced Studies
Aarhus Universitet
bpp@mbg.au.dk; 29723499
