All folding is good when it gets off to a good start
Aarhus researchers are behind the most detailed description of how membrane protein folds. This provides new knowledge about the wonderful world of membrane proteins.
For the last three decades, intense work has been carried out to understand how proteins fold, i.e. how they achieve their fine three-dimensional structure – which is also the basis for their biological function, regardless of whether it concerns metabolism, signal transfer or structure. The greatest progress by far has been made in water-soluble proteins, which are generally quite straightforward to work with.
Read more (in Danish only) below. For contact details in English, go to the bottom of the page.
Derimod halter det langt bagefter med at forstå foldningen af membranproteiner, altså de proteiner som ligger dybt integreret i cellemembranen – den tynde (ca. 3-5 nm tykke) fedthinde der adskiller cellens indre fra dets ydre. Disse proteiner er grundvidenskabeligt interessante fordi de netop er ”programmeret” til at folde i et fedtholdigt miljø, snarere end et vandopløseligt ditto – så spillereglerne forventes at være anderledes, selvom de overordnede principper nødvendigvis må være de samme som for de vandopløselige proteiner. Samtidig er membranproteiner – særligt de der danner såkaldte a-helix (spiralformede) strukturer - meget interessante, fordi de regulerer transport ind og ud af cellerne (jvf den flotte tradition for at arbejde med ion-pumper på Aarhus Universitet som Jens Chr. Schou fik Nobelprisen for), og er derigennem mål for mange lægemidler.
Membranproteiner stiller krav
Problemet er at membranproteiner er meget svære at arbejde med, netop fordi de stiller store krav til deres omgivelser for at folde: de skal hele tiden befinde sig i et miljø, der minder om membranen. Det betyder, at de meget let klumper sammen og bundfælder, hvis de ikke bliver behandlet ordentligt, og normalt har cellen svært ved at producere dem i store mængder, eftersom der er meget mindre plads i membranen end i cellens cytosol. Der skal også særlige tricks til for at sikre, at man kan måle foldning af disse proteiner: proteinet skal først ”nulstilles”, dvs. udfoldes så det mister sin biologisk aktive struktur, på en måde der undgår at det klumper sammen, og så skal foldningsprocessen sættes i gang på en eller anden måde. Mange membranproteiner har simpelthen svært ved at folde i reagensglasset (in vitro)fordi det er nærmest umuligt at genskabe cellens foldningsbetingelser in vitro. Der er derfor indtil videre kun 2 a-helix membranproteiner man har undersøgt grundigt på denne måde, nemlig ”arbejdshesten” bacteriorhodopsin (bR) fra den purpur-farvede membran af Archaebakterien Halobacterium salinarum og det lille membranprotein DsbB fra E. coli. Begge proteiner er lidt specielle – bR kræver et hjælpestof (retinal) for at folde, og DsbB danner svovlbroer internt og har en ret kompliceret foldningsvej.
Succes med at folde besværligt protein
Vi har netop udgivet en artikel i det anerkendte tidsskrift Proceedings of the National Academy of Sciences of U.S.A. der udgør velnok den mest detaljerede beskrivelse af et membranproteins foldning – tilmed et meget enkelt foldningsmønster. Det drejer sig om membranproteinet GlpG, som findes i E. coli (ligesom DsbB) men derudover har slægtninge i højere organismer, der er involveret i sygdomme som diabetes og kræft. Det er lykkedes os - Daniel Otzen, ph.d.-studerende Wojciech Paslawski (nu postdoc på Karolinska Institutet) og Otzens forskergruppe på iNANO - at udvikle metoder til at følge både foldning og udfoldning af GlpG under betingelser ,der minder om membranen. Metoden benytter overfladeaktive stoffer (tensider), som kan kombineres i forskellige forhold for enten at folde eller udfolde proteinet. Det viser sig at GlpG’s foldning er meget simpel – den går simpelthen lige fra den udfoldede tilstand til den native tilstand uden andre ”rastepladser” på vejen. Det betyder, at hvis man skal forstå hvordan den folder, skal man bare undersøge hvordan proteinets foldningstransitionstilstand ser ud – altså den tilstand der udgør barrieren for foldning. Når proteinet er kommet ”op” til TS’en, foregår resten af foldningen utroligt hurtigt, så TS’en er så at sige flaskehalsen for foldningsprocessen.
Indirekte målinger og hestearbejde
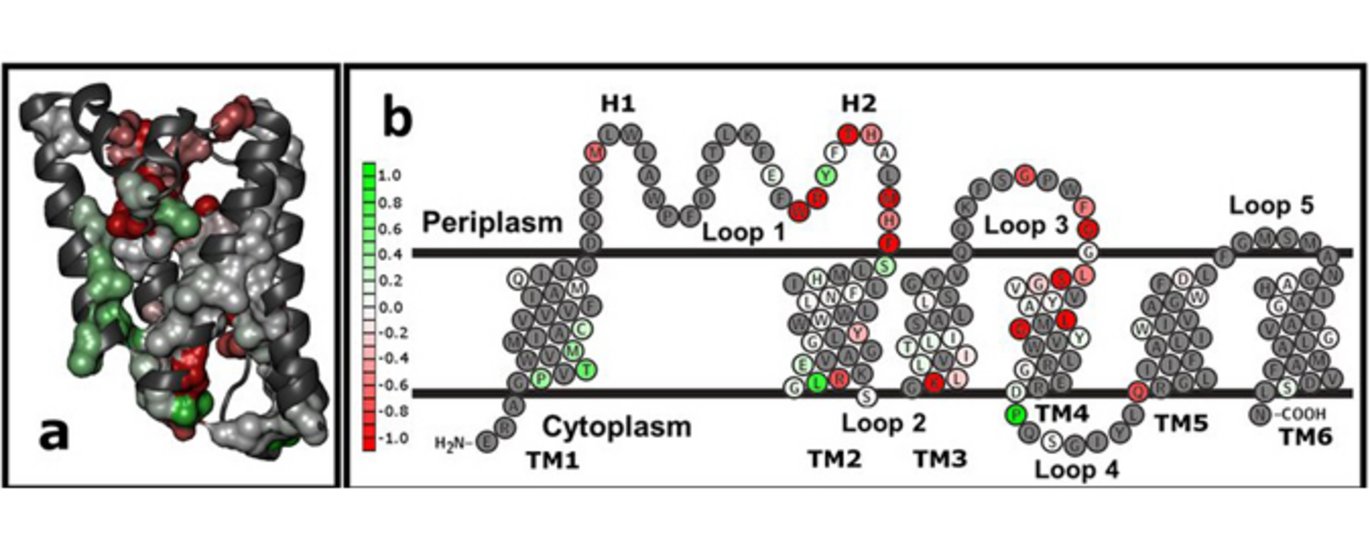
TS’en kan man ikke måle direkte: man er nødt til at måle hvor hurtigt proteinet folder og udfolder. For at finde ud af hvilke dele af proteinet folder først, laver man systematiske udskiftninger (enkeltmutationer af individuelle sidekæder) rundt omkring i proteinets struktur og måler hvor hurtigt disse mutanter folder og udfolder. Den del af proteinet der folder først (”foldningskernen”), vil være mest følsom overfor disse ændringer og derfor folde langsommere, når de bliver ændrede. Det har været et rigtigt hestearbejde: vi har lavet omkring 70 mutanter og målt på dem en ad gangen. Klonerne har vi fået af vores gode samarbejdspartner Sin Urban fra Johns Hopkins Universitet i USA, og alle mutanterne er blevet oprenset af min laborant Ove Lillelund, som er blevet gruppens membranprotein ekspert. Arbejdet har heldigvis båret frugt. Det viser sig nemlig, at foldningsmønstret er ret simpelt: det er ”begyndelsen” af proteinet (de første 2 helicer ud af de 6 helicer som GlpG indeholder) der folder først, ganske ligesom det er denne del af proteinet der først ”spyttes ud” i cellemembranen, når proteinet laves i cellen. Det ser altså ud til at proteinet simpelthen er programmet til at folde på en måde som afspejler hvordan den laves i cellen – bagenden af proteinet (de sidste 4 helicer) venter helt med at folde indtil kernen er på plads.
Mærkelige løkker overfolder
Der er dog ét særlig ”twist” ved historien: de løkker som forbinder de to helicer i foldningskernen opfører sig ret mærkeligt. Det ser ud til at de er ”overfoldede” i TS, så de rent faktisk folder hurtigere, når de muteres, stik mod ”god opførsel”. Måske hænger det sammen med at helicerne også skal være rigtigt placeret i forhold til hinanden for at folde og det kræver at løkkerne skal ”strække” sig på en lidt anderledes måde. Interessant nok viser det sig at proteinet DsbB, som vi også stod for at undersøge, har tilsvarende ”overfoldede” områder i en bestemt del af membranproteinet. Måske er denne overfoldning ligefrem en del af disse særlige membranprotein spilleregler – sammen med den regel at begyndelsen folder først. Det kræver selvfølgelig yderligere undersøgelser at finde ud af. Heldigvis er der god mulighed for det. Jeg har for nyligt ansat postdoc Nicholas Schafer til at finde ud af om måleresultaterne kan bruges til til at udvikle en god computermodel der kan genskabe foldningen af GlpG i computeren. Det forsøg udføres sammen med lektor Kresten Lindorff-Larsen på Københavns Universitet. Og derefter skal man så prøve at udvikle metoder til at følge foldningen i rigtige celle membraner. Men det må betragtes som en langtidsinvestering på linje med et større boliglån– og så håber vi selvfølgelig ikke at forskningsrenten stiger
Artikel:
Paslawski, W., Kristensen, J. V., Lillelund, O., Schafer, N., Baker, R., Urban, S., and Otzen, D. E. (2015) Cooperative folding of a polytopic ?-helical membrane protein involves a compact N-terminal nucleus and non-native loops, Proc. Natl. Acad. Sci. USA8. juni 2015.
Contact
Professor Daniel Otzen
Department of Molecular Biology and Genetics/iNANO
Aarhus University, Denmark
E-mail dao@inano.au.dk, phone +45 20725238.
