Aarhus-forskere løser mysterium i blodet
En tværfaglig gruppe af forskere fra AU har netop publiceret en artikel i Nature med titlen ”Structure of the haptoglobin–haemoglobin complex". Lektor Gregers Rom Andersen fra MBG har bidraget til artiklen med at bestemme krystalstrukturen af komplekset mellem hæmoglobin og haptoglobin.
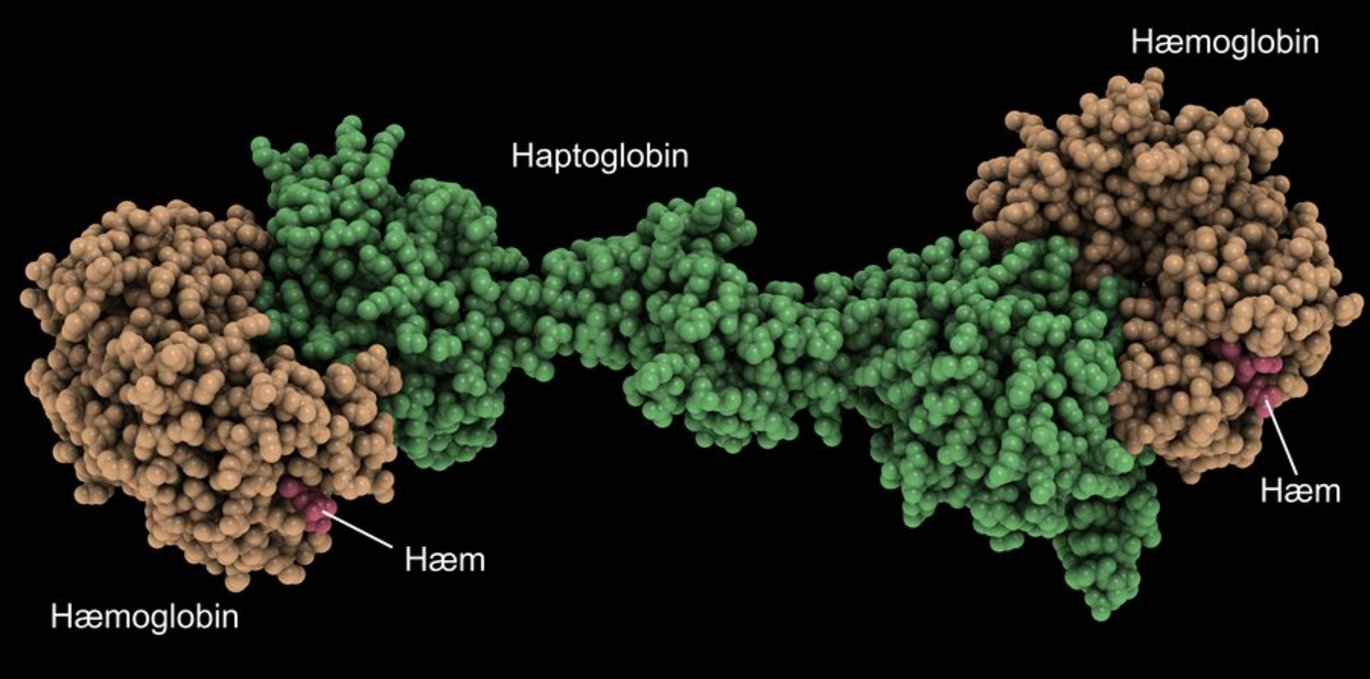
Forskere fra forskningscentret MEMBRANES ved Aarhus Universitet har fundet den afgørende brik i et videnskabeligt puslespil, som siden 60’erne har været anset for umulig at gøre færdigt: at finde strukturen for det beskyttende proteinkompleks som dannes, når blodets hæmoglobin frigøres fra røde blodlegemer. Dette sker ved en række sygdomme som f.eks. malaria.
Opdagelsen er en 3-dimensional kortlægning af det, der i fagsprog hedder ’ haptoglobin-hæmoglobin komplekset’, og den er netop er blevet publiceret i det internationalt førende tidsskrift Nature.
”Vores gennembrud kom, da vi efter en række mislykkede forsøg med menneskeblod gik på slagteriet efter griseblod. Det var jo ikke et specielt højteknologisk indfald, men det var, hvad der skulle til… et lille hop over i et dyr, der ligner mennesket, og så virkede det hele pludseligt efter to år med meget mere komplicerede genteknologiske, men mislykkede, forsøg”, fortæller leder af forskningsgruppen, professor dr. med. Søren Kragh Moestrup, Institut for Biomedicin.
Opdagelsen giver ny viden om det vigtige hæmoglobin, som de røde blodlegemer er spækket med. Hæmoglobin er nødvendigt for kroppen, fordi det transporterer ilt i blodet. Men det bliver giftigt og kan forårsage skade på væv og ikke mindst nyrerne, når det frigøres fra cellerne, hvilket bl.a. sker ved sygdom og infektioner. Imidlertid kan et andet protein, haptoglobin, indfange og danne kompleks med hæmoglobinet og føre det hen til en receptor, som indfanger og sluger det. Receptoren ved navn CD163 blev i sin tid opdaget i samme forskningsgruppe.
”Nu har vi vist, hvordan dette unikke og stærke proteinkompleks opstår, da det er lykkedes os at generere et 3-dimensionelt kort over atomerne ved hjælp af røntgen-krystallografi. Så nu kan man for første gang se, hvordan de to proteiner helt præcist sidder sammen i komplekset”, fortæller ph.d. Christian Brix Folsted Andersen, der sammen med specialestuderende Morten Torvund-Jensen har haft afgørende indflydelse på arbejdet.
Resultaterne har desuden ført til opdagelse af en hel ny type proteinstruktur, hvis anvendelse universitetet har ansøgt om patent på. Opdagelsen har bl.a. nye perspektiver for fremstilling af kunstige proteiner til brug for diagnostik og behandling.
Se artiklen i Nature
MEMBRANES er et forskningscenter ved Aarhus Universitet med fokus på de proteiner, der har en funktion i en cellemembran.
Projektet er et interdiciplinært og internationalt samarbejde udgået fra Institut for Biomedicin, Aarhus Universitet, med deltagelse af forskere fra Science & Technology, Aarhus Universitet, samt eksperter fra Norge og Brasilien.
Arbejdet er finansieret af midler fra Lundbeckfonden, Novo Nordisk Fonden, Norges Forskningsråd, The European Research Council og Det Frie Forskningsråd - Sundhed og Sygdom.
Yderligere oplysninger:
Professor, dr. med. Søren Kragh Moestrup, MEMBRANES, Institut for Biomedicin, Aarhus Universitet. Mobil 28 99 22 82; sm@biokemi.au.dk
Adjunkt, ph.d. Christian Brix Folsted Andersen, MEMBRANES, Institut for Biomedicin, Aarhus Universitet. Mobil 30 26 48 55; cbfa@biokemi.au.dk
