Et lille protein med mange anvendelsesmuligheder
Forskere fra Institut for Molekylærbiologi og Genetik samt Institut for Biomedicin på Aarhus Universitet har i samarbejde udviklet og beskrevet et lama-antistof, som potentielt kan have stor betydning for fremtidens diagnosticering og behandling af bl.a. nyresygdomme.
Forskerne har studeret et protein kaldet C3 fra den del af vores medfødte immunsystem, der kaldes komplementsystemet. Når immunsystemet genkender sygdomsfremkaldende organismer eller vores egne døende celler, kløves C3 af enzymer i blodet som led i en forsvarsmekanisme. Disse enzymer kaldes C3 konvertaser, og kløvningen af C3 resulterer i to fragmenter. Det ene, kaldet C3b, binder direkte til de sygdomsfremkaldende organismer, mens det andet rekrutterer og stimulerer immunceller til at eliminere skadevolderen.
I en rask person er vores egne celler beskyttet mod effekterne af C3 kløvning. Men denne beskyttelse kan delvist mistes f.eks. som følge af mutationer i vores DNA, og herved opstår der risiko for at udvikle kroniske betændelsestilstande og autoimmune sygdomme. Derfor har der længe været et stort fokus på udvikling af stoffer, som kan bruges til at forhindre uønsket komplementaktivering. Forskerne udviklede derfor lama-antistoffet for at forhindre kløvning af C3. Lama-antistoffer kaldes også nanobodies på grund af deres meget lille størrelse, og sammenlignet med normale antistoffer er nanobodies nemme at udvikle og væsentligt billigere at producere.
”Teknologien hvorved nanobodies udvikles og produceres har været kendt i mere end to årtier,” siger Gregers Rom Andersen og supplerer, ”derfor er det også lidt overraskende at vi, efter vores bedste overbevisning, er de første i verden som beskriver udvikling et nanobody, der kan hæmme komplementsystemet.”
Ved at beskyde krystaller med røntgenstråling og sammenligne med data fra elektronmikroskopi har forskerne beskrevet meget detaljeret hvordan deres nanobody binder til C3.
”Krystalstrukturen af vores nanobody bundet til C3 understøtter vores tidligere modeller for, hvordan konvertaserne i komplementsystemet genkender deres substrat og forklarer derfor, hvorfor vores nanobody virker hæmmende på kløvningen af C3. Disse resultater forbedrer dermed også vores grundvidenskabelige forståelse af, hvordan dette essentielle step i komplementsystemet fungerer. Ved at sammenligne med tidligere publicerede proteinstrukturer kan vi også forstå, hvorfor vores nanobody ydermere forhindrer dannelsen af C3 konvertaserne, det her nanobody er så at sige dobbelthæmmende,” forklarer Rasmus Kjeldsen Jensen.
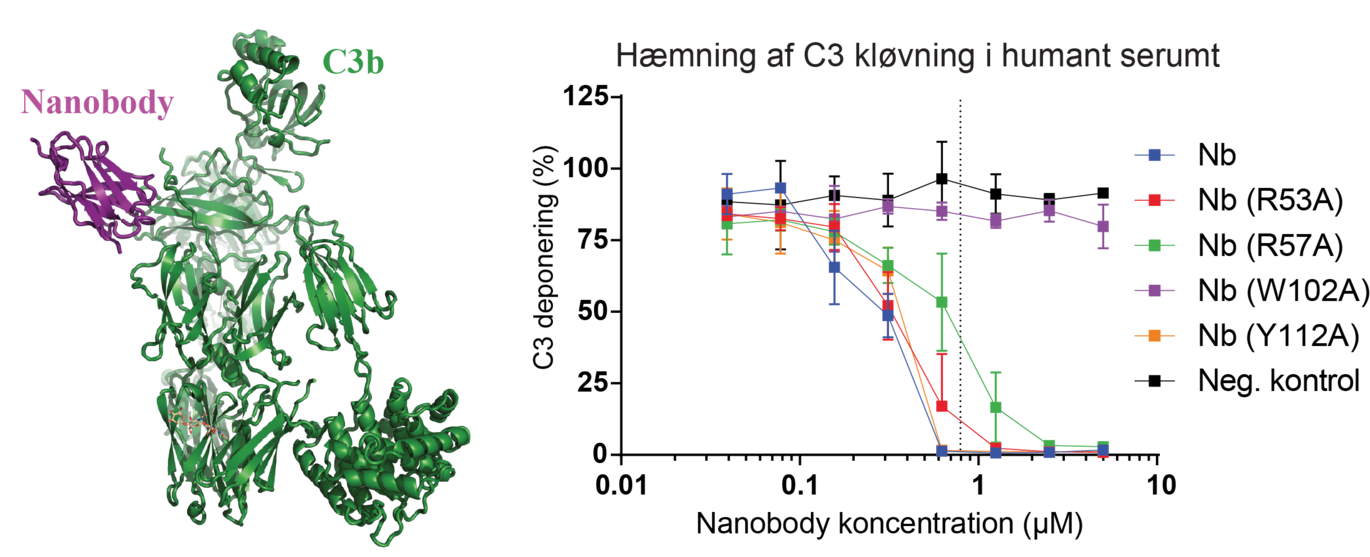
Den nyudviklede antibody kan forhindre kløvning af C3-proteinet
Udover arbejdet med at beskrive strukturen af nanobody-C3 komplekset har forskerne også udført mange laboratorieforsøg i serum fra både mus og mennesker. Disse resultater understøtter observationerne fra strukturen og viser tydeligt, at deres nyudviklede nanobody kan forhindre kløvningen af C3 i både mennesker og mus. Det sidste er vigtigt, da mus ofte anvendes som sygdomsmodeller.
”Vores forsøg i serum er vigtige for at demonstrere at vores nanobody faktisk virker, der hvor komplementsystemet fysiologisk udøver sin aktivitet. Disse resultater peger på, at vores nanobody vil kunne bruges i behandling af sygdomme, hvor komplementsystemet er overaktivt. Som eksempel er en del af nyren ikke beskyttet mod komplement i samme grad som andre væv, og her kunne vores nanobody være en kandidat til at standse kendte sygdomstilstande i nyren forårsaget af komplement,” siger Gregers Rom Andersen. ”Der er dog et lille aber dabei - vores nanobody viser sig nemlig også at kunne undertrykke en af de beskyttende effekter vores krop normalt udøver på komplement, og man skal derfor være meget forsigtig og omhyggeligt vurdere faren for at bruge vores nanobody i en eventuel sygdomsbehandling,” slutter Gregers Rom Andersen.
Grundlaget for projektet var etableret af adjunkterne Kasper Røjkjær Andersen og Nick Stub Laursen fra Institut for Molekylærbiologi og Genetik, der som de første i Danmark har opsat systematisk udvikling og produktion af nanobodies i stor stil. Men den drivende kraft i projektet var ph.d.-studerende Rasmus Kjeldsen Jensen under vejledning af professor Gregers Rom Andersen, som i karakteriseringen af antistoffet fik assistance af de to ph.d.-studerende Trine Amalie Fogh Gadeberg og Rasmus Pihl.
De opnåede resultater er netop blevet offentliggjort i det anerkendte tidsskrift Journal of Biological Chemistry.
Rasmus K Jensen, Rasmus Pihl, Trine A.F. Gadeberg, Jan K. Jensen, Kasper R. Andersen, Steffen Thiel, Nick S Laursen and Gregers Rom Andersen: A potent complement factor C3 specific nanobody inhibiting multiple functions in the alternative pathway of human and murine complement.
Baggrundsinformation
Mere information
Professor Gregers Rom Andersen
Institut for Molekylærbiologi og Genetik
Aarhus Universitet
gra@mbg.au.dk
+45 30256646
