Danske forskere afslører hvordan MRSA-bakterien håndterer stress
Et internationalt forskerhold har klarlagt en grundlæggende mekanisme, der er ansvarligt for stafylokokbakteriens håndtering af stress, når den udsættes for antibiotika. Det forventes, at forskningsresultaterne på sigt vil kunne bruges til at udvikle nye antibiotika, der omgår stressmekanismerne.
Forståelse af bakteriers stressmekanismer er af stor betydning for vores evne til at behandle bakterielle infektioner, da disse mekanismer ofte tillader bakterierne at overleve antibiotikabehandlingen. En gruppe forskere ved Institut for Molekylærbiologi og Genetik ved Aarhus Universitet har nu i samarbejde med forskere ved Københavns Universitet, Umeå Universitet i Sverige, og Tartu Universitet i Estland, klarlagt en grundlæggende mekanisme, hvormed Stafylokok-bakterien, der er ansvarlig for MRSA (methicilinresistente stafylokokker), håndterer stress, f.eks. når den udsættes for antibiotika.
De nye forskningsresultater, der netop er publiceret i det amerikanske tidsskrift Journal of Biological Chemistry, viser hvordan bakterierne danner et bestemt enzym, der er i stand til at modificere nogle af de byggeblokke, der normalt bruges til arvematerialet DNA, og i stedet omdanne dem til signalmolekyler, der signalerer stress. Når bakterierne udsættes for f.eks. antibiotikabehandling, vil der derfor dannes store mængder af disse signalmolekyler, hvilket betyder at bakteriens vækst sættes i stå, og cellerne går i dvale. I denne dvaletilstand er de ikke så modtagelige overfor antibiotika og er dermed i stand til at overleve.
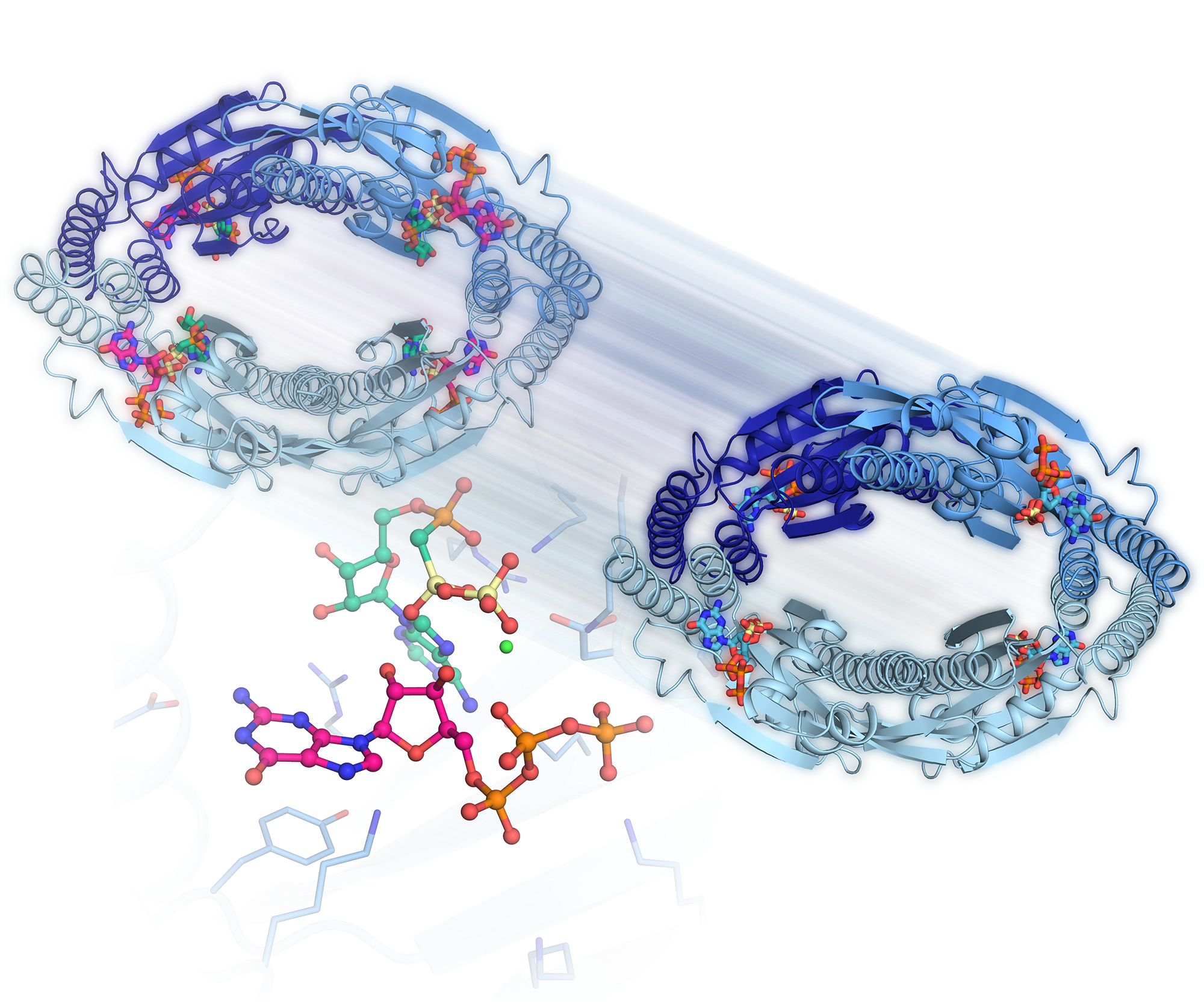
Forskerne fra Aarhus Universitet, der har arbejdet under ledelse af lektor Ditlev E. Brodersen, har benyttet en raffineret eksperimentel teknik til at opstille præcise tredimensionelle modeller for enzymets tilstand, lige før og lige efter det har dannet et signalmolekyle. Modellerne, der er præcise helt ned til det atomare niveau, afslører hvordan enzymet deltager i reaktionen, der leder til dannelse af signalmolekylet. Samtidig kunne forskerne se, at fire enzymer går sammen og danner en cirkel inde i bakteriecellerne, og på den måde er i stand til at kommunikere med hinanden. Den nye mekanisme kan betyde, at dannelsen af signalstoffer forøges kraftigt under antibiotikabehandling, hvorved effekten bliver så meget desto større. Det forventes at forskningsresultaterne på sigt vil kunne bruges til at udvikle nye antibiotika, der omgår stressmekanismerne.
Link til artiklen i Journal of Biological Chemistry med titlen "Structural basis for (p)ppGpp synthesis by the Staphylococcus aureus small alarmone synthetase RelP".
Mere information
Lektor Ditlev E. Brodersen
Institut for Molekylærbiologi og Genetik, Aarhus Universitet
deb@mbg.au.dk - 2166 9001
