Ny opdagelse fra det molekylære maskinrum for depression og afhængighed
Forskere ved Aarhus Universitet har beskrevet, hvordan en gruppe af hjernens transportproteiner med vigtige roller i depression og afhængighed overvinder det trin, der begrænser deres effektivitet. Opdagelsen gør det muligt at beskrive transportproteinets fulde funktion og kan give bedre muligheder for at modvirke amfetamins og ecstasys effekt på hjernen.
Når nerveceller skal kommunikere med hinanden i vores hjerner, sker det ved at frisætte små signalmolekyler, såkaldte neurotransmittere, der virker som kemiske sendebude i særlige kontaktpunkter mellem nervecellerne, kaldet synapser. Her bindes og registreres den frisatte neurotransmitter af receptorer på modtager-nervecellens overflade, som så igen udløser et signal, der sendes videre til andre nerveceller. De kredsløb i hjernen, der betjener sig af neurotransmitterne noradrenalin, dopamin, GABA og serotonin vides at spille en vigtig rolle for humør, belønning og psykisk velbefindende, ligesom de også er centrale i psykiske lidelser som afhængighed og depression.
Efter frisætningen af neurotransmittere mellem nerveceller skal de dog fjernes igen for at afslutte signalet. Det sker ved, at en familie af transportproteiner virker som molekylære støvsugere i nervecellens cellemembran, hvor de pumper neurotransmitteren tilbage i nervecellen til senere genbrug. Denne transport har stor betydning for signaleringen mellem nervecellerne, men sker relativt langsomt. Et samarbejdsprojekt mellem forskere fra Institut for Molekylærbiologi og Genetik, Klinisk Institut og Institut for Kemi har gjort det muligt at forklare, hvad der sker i det afgørende hastighedsbegrænsende trin i transportprocessen for neurotransmittere som serotonin, noradrenalin, GABA og dopamin, som alle transporteres af beslægtede proteiner med samme mekanisme.
Kompliceret og energikrævende proces
Transport af vandopløselige neurotransmittere over en fedtholdig cellemembran er en kompliceret proces, som udfordres på samme måde som det at blande vand og olie. Processen er også energikrævende, da transportproteinerne skal arbejde mod en ophobning af neurotransmittere inde i cellen - ligesom det kræver energi at pumpe luft i en cykelslange. Drivkraften til denne neurotransmitters pumpeproces kommer fra natriumioner, som følger med neurotransmitteren, men som omvendt går fra en høj koncentration uden for cellen til en meget lav koncentration inde i cellen. Pumpeprocessen drives således af en strøm baseret på natriumioner. Af samme grund er det essentielt, at transportprocessen ikke kortsluttes ved, at natriumioner transporteres uden neurotransmitter, eller på anden måde lækker ioner.
Neurotransmittertransporterens første opgave er derfor at binde et neurotransmittermolekyle fra nervecellens yderside sammen med to natriumioner til et bindingssted midt i proteinet. Når de er på plads, kan transporteren udføre en dramatisk bevægelse, så bindingsstedet lukkes mod ydersiden af nervecellen og i stedet åbner mod nervecellens indre, hvor neurotransmitteren og natrium afgives. For at transporteren igen kan eksponere sit bindingssted til nervecellens ydre for at udføre en ny runde af transport, er den dog først nødt til at foretage en modsat bevægelse, nemlig fra indadvendt til udadvendt, men uden neurotransmitter og natriumioner. Denne ændring er den hastighedsbegrænsende faktor for, hvordan fx serotonintransporteren fungerer. Det har stor betydning for den overordnede tid, som et neurotransmittersignal fungerer i. Transporteren har med andre ord tendens til at blive hængende i denne indadvendte tilstand, og stoffer som amfetamin og ecstasy virker ved at kapre transporteren i netop denne tilstand og få den til at køre baglæns i stedet, så den pludselig og ukontrollabelt frisætter neurotransmittere i stedet for at fjerne dem.
Transporterens bevægelsesstrategi
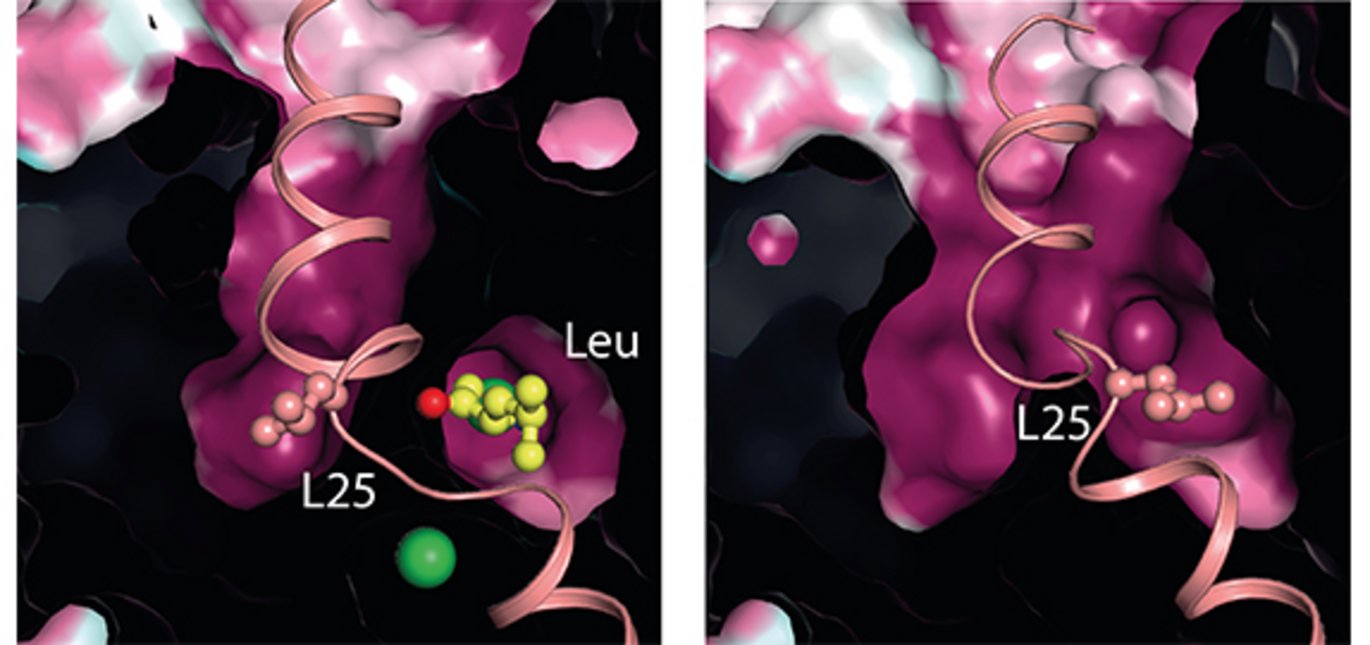
Ved at løse den molekylære struktur for et nært beslægtet protein til disse neurotransmittertransportere, som befinder sig i en tilstand under returbevægelsen fra indadvendt til udadvendt, er det nu blevet tydeligt, hvordan transporteren løser problemet med at bevæge sig uden natriumioner og neurotransmitter. Et centralt placeret og komplet bevaret element af transportere af denne type foretager nemlig en rotation, der dels placerer dette element i den tomme bindingslomme for neurotransmittere, og dels forvrænger natriumionernes bindingssteder. Biokemiske eksperimenter samt computersimuleringer viser, at denne rotation gør det muligt for transporteren af bevæge sig tilbage til den udadvendte tilstand og samtidig ikke vil binde natriumioner, før det roterede element er roteret tilbage. Dermed sikres det, at transporteren ikke lækker natriumioner ved at gå baglæns i denne proces. Forskerne har tillige vist, at hvis dette roterende element ændres bare minimalt, så fungerer transporteren ikke ordentligt og kan ikke udføre sin funktion.
Denne nye forståelse af neurotransmittertransporternes mekanisme giver håb om bedre muligheder for at behandle depression, overdosis og afhængighed, da vi nu bedre forstår, hvordan lægemidler og stoffer som ecstasy og kokain, som binder til disse transportere i forskellige tilstande, skal gøre dette for at opnå den rette effekt.
Den videnskabelige artikel er netop publiceret i Nature Communications.
Lina Malinauskaite, Saida Said og Caglanur Sahin er alle førsteforfattere på studiet, og de er nu videre i deres karriere: Lina Malinauskaite er ansat som postdoc ved Oxford University, Saida Said er ph.d.-studerende ved AU, mens Caglanur Sahin er kemiker hos Novo Nordisk.
Projektet har været ledet af Poul Nissen, Institut for Molekylærbiologi og Genetik, Steffen Sinning, Institut for Klinisk Medicin og Birgit Schiøtt, Institut for Kemi, alle Aarhus Universitet.
Se movie med beskrivelse af processen (Movie: Lina Malinauskaite).
Mere information
Professor Poul Nissen
Institut for Molekylærbiologi og Genetik/Danish Research Institute of Translational Neuroscience—DANDRITE
Aarhus Universitet
pn@mbg.au.dk - mobil: 28992295
Adjunkt Steffen Sinning
Institut for Klinisk Medicin
Aarhus Universitet
steffen.sinning@clin.au.dk - mobil: 40768836
Professor Birgit Schiøtt
Institut for Kemi
Aarhus Universitet
birgit@chem.au.dk - mobil: 29826882