Ion- og lipidtransportører har fundet deres egen niche
For at en celle kan overleve kræves det, at en række funktioner ved cellemembranen opretholdes korrekt. Ion- og lipidpumperne kaldet P-type ATPases er med til at skabe denne balance ved at transportere substrater hen over membranen, og de har udviklet sig til forskellige typer, der tager sig af specifikke substrater inden for forskellige områder. Nye studier viser nu, hvordan to meget vigtige typer P-type ATPaser har tilpasset sig forskellige substrater og fysiske miljøer, og på den måde indgår i cellers centrale processer for at opretholde liv.
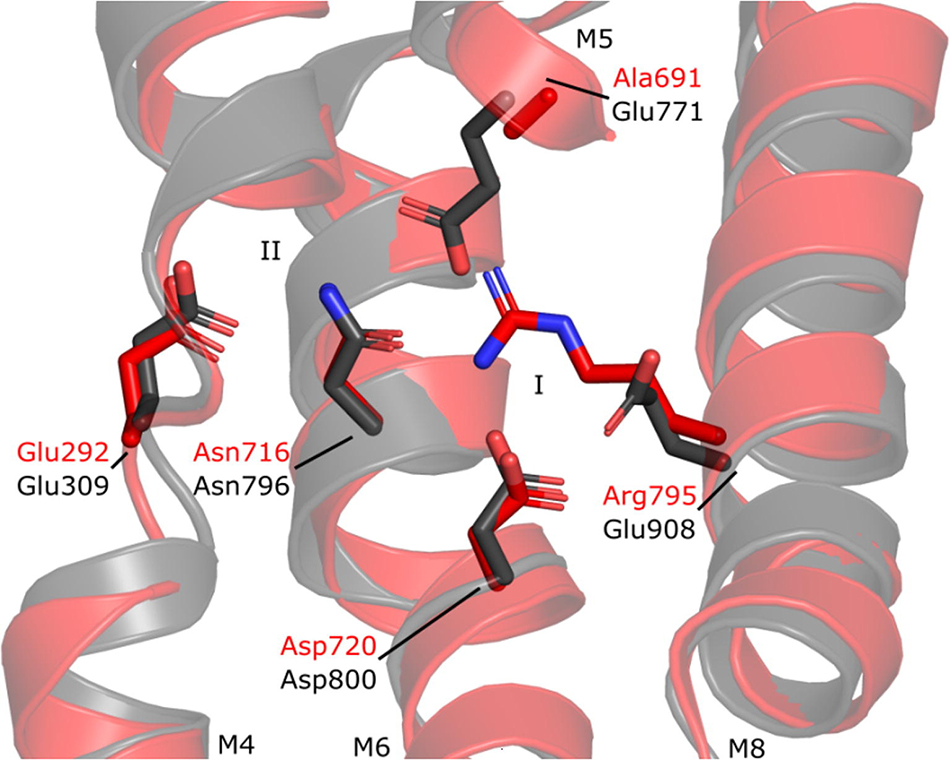
Mange bakterier eksporterer calcium ind i cellen ved hjælp af aktive transportører, der er identiske med de kendte Ca2+-ATPase fra pattedyr, såsom plasmamembran Ca2+-ATPase og den såkaldte sarco-endoplasmisk reticulum Ca2+-ATPase (henholdsvis PMCA og SERCA). Krystalstrukturer af Ca2+-ATPase 1 fra bakterien Listeria monocytogenes (LMCA1) antyder, at LMCA1 er tilpasset til hurtigt at fjerne fosforylering efter frigivelse af Ca2+, hvilket kan forklare tidligere enkelt-molekyle observationer af LMCA1 dynamik.
Variation i arkitekturen på calciumbindingsstederne forklarer også, hvorfor LMCA1 transporterer en enkelt Ca2+ ion lige som PMCA, men i modsætning til to transporterede Ca2+ ioner i SERCA. LMCA1-strukturer viser den evolutionære forskel og de bevarede træk ved denne vigtige klasse af iontransportører, der således også informerer os om centrale mekanismer i Ca2+-ATPaser fra pattedyr, og hvordan de kan reguleres eller påvirkes af patologiske tilstande.
For P4-ATPase-studierne tog forskerne et andet perspektiv. Transportcyklussen for en P-type ATPase består af to halvreaktioner: Først en fosforylering, hvor et fosfat overføres fra ATP til transportøren, og så en defosforylering, hvor fosfatet frigives igen. I modsætning til iontransportører, såsom førnævnte LMCA1, transporterer P4-ATPaser lipider og betegnes også lipid flippaser. Hvor Ca2+ transporten i LMCA1 er koblet til fosforylerinssreaktionen efterfulgt af defosforylering, er lipidtransporten omvendt, koblet til defosforyleringsreaktionen i cyklussen efterfulgt af fosforylering.
Ved hjælp af nye strukturer bestemt ved kryo-elektronmikroskopi (cryo-EM) af en lipid-flippase fra gær, kaldet Drs2p-Cdc50p, blev det undersøgt, hvordan lipid-flippaserne afviger fra iontransportører og har ”flippet” den enzymatiske mekanisme i fosforylering-defosforyleringscyklus. Cryo-EM-teknikken for været afgørende for disse studier, og flere strukturer i transportcyklussen kunne bestemmes ved at låse Drs2p-Cdc50p ved hjælp af forskellige hæmmere. Elektronmikroskopidata blev indsamlet ved den nationale elektronmikroskopi-infrastrukturfaciliteten ved Aarhus Universitet (EMBION).
Ph.d.-studerene Sara Basse Hansen og postdoc Milena Timcenko har stået i spidsen for de to studier (under vejledning af professor Poul Nissen; Sara Basse tillige af lektor Magnus Kjærgaard), og artiklerne er offentliggjort i Journal of Molecular Biology, som er et af de ældste tidsskrifter i molekylærbiologi og strukturbiologi.
Link til de to videnskabelige artikler i Journal of Molecular Biology
The Crystal Structure of the Ca2+-ATPase 1 from Listeria monocytogenes reveals a Pump Primed for Dephosphorylation
Sara Basse Hansen, Mateusz Dyla, Caroline Neumann, Esben Meldgaard Hoegh Quistgaard, Jacob Lauwring Andersen, Magnus Kjaergaard & Poul Nissen
Structural basis of substrate-independent phosphorylation in a P4-ATPase lipid flippase: Milena Timcenko, Cédric Montigny, Thomas Boesen, Joseph A. Lyons, Guillaume Lenoir & Poul Nissen
Mere information
Ph.d.-studerende Sara Basse Hansen - sarabasse@mbg.au.dk
Postdoc Milena Timcenko - MIT@bio.ku.dk - +45 35 33 28 95
Professor Poul Nissen – pn@mbg.au.dk - +45 2899 2295
DANDRITE/Institut for Molekylærbiologi og Genetik, Aarhus Universitet
