Udvikling af nyt system kan effektivisere kræftbehandling
Forskere ved Molekylærbiologisk Institut på Aarhus Universitet har udviklet et nyt cellulært system, som gør det muligt nøje at følge reparation af specifikke skader i arvemassen, som opstår, når kræftceller behandles med kemoterapeutika rettet mod en gruppe enzymer kaldet topoisomeraser. Disse stoffer hører til de mest succesfulde kemoterapeutiske stoffer, som i dag anvendes i behandling af kræft. Systemet vil gøre det muligt at udvikle strategier for en mere målrettet og effektiv behandling af kræftceller end hidtil.
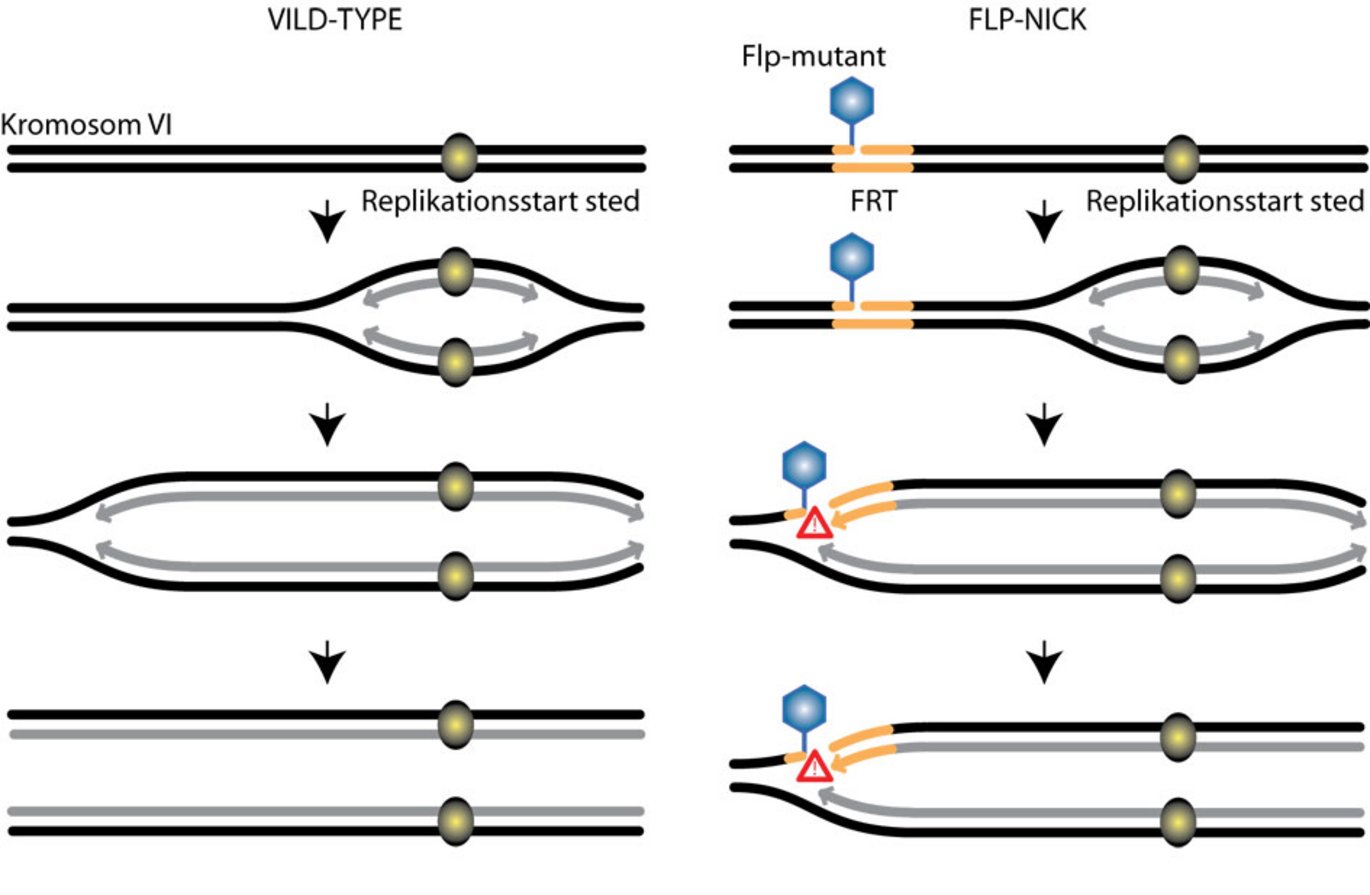
Venstre side viser en normal situation (vildtype), hvor dna-syntesen (dna replikationen) påbegyndes ved et veldefineret replikationsstartsted og forløber uden problemer. Højre side viser Flp-nick systemet, hvor en FRT-sekvens er indsat i genomet. Under kløvning vil Flp-mutanten danne et stabiliseret kløvningskompleks ved FRT-sekvensen, som omdannes til et permanent brud, når replikationsapparatet kolliderer med kløvningskomplekset.
Forskernes resultater er netop publiceret i det anerkendte, internationale tidsskrift Nature Methods.
Baggrundsinformation
Dna'et udgør som bekendt vores arvemasse og består af to strenge vundet omkring hinanden i en dobbeltspiral. Når dna'et skal kopieres inden celledelingen, adskilles de to dna-strenge, så der bliver adgang til den genetiske information. Pga. dna'ets struktur leder dette til vridninger i dna'et, som skal fjernes, for at kopieringen kan forløbe uden problemer. Dette varetages af en gruppe enzymer - kaldet dna-topoisomeraser - der laver midlertidige brud i dna-spiralen. Under processen bliver enzymerne bundet til dna'et i et kløvningskompleks, inden bruddet igen lukkes. Dette udnyttes af en vigtig gruppe kræftkemoterapeutika, idet de fanger enzymerne i kløvningskomplekset og forhindrer, at dna-bruddene lukkes.
De stabiliserede kløvningskomplekser kan omdannes til permanente brud, hvis proteinkomplekser - som enten kopierer dna'et eller oversætter dna'et til rna for at videregive den genetiske information til proteinsyntese - kolliderer med kløvningskomplekserne. Kræftkemoterapeutika rettet mod topoisomeraser dræber således kræftceller ved at fragmentere arvemassen. Dette udnyttes i behandlingen af flere forskellige kræftformer bl.a. livmoderhalskræft, æggestokkekræft samt visse former for lungekræft og leukæmi. Cellens respons på behandling med disse kemoterapeutika er at begynde en reparation af skaderne i arvemassen. Effektiviteten af en kemoterapeutisk behandling afhænger derfor i høj grad af cellens kapacitet til at fjerne de akkumulerede kløvningskomplekser, inden de ændres til permanente brud. En målrettet hæmning af de involverede reparationsfaktorer vil derfor øge effektiviteten af den kemoterapeutiske behandling.
Det nyudviklede system
Systemet, som kaldes det cellulære Flp-nick system, gør det muligt at undersøge reparation af et enkelt kløvningskompleks lokaliseret et specifikt sted i arvemassen, hvilket hidtil ikke har været muligt. For at skabe en situation i cellen, som efterligner et medicinstabiliseret topoisomerasekløvningskompleks, har forskerne anvendt et enzym (kaldet Flp), som har en katalytisk mekanisme, der ligner topoisomerasens, idet det laver midlertidige brud i dna'et. Enzymet, som anvendes i det cellulære Flp-nick system, er muteret således, at det ikke længere kan lukke dna-bruddet, og derved dannes et stabiliseret kløvningskompleks.
Enzymet har yderligere den fordel, at det kløver ved veldefinerede dna-sekvenser, hvorved kløvningen kan målrettes til et specifikt sted i genomet ved at indsætte genkendelsessekvensen (kaldet FRT). Udtrykket (også kaldet ekspressionen) af enzymet kontrolleres vha. en specifik promoter, som kan tændes og slukkes afhængig af vækstmedium.
Hidtil har cellulære studier vedrørende reparation af de skader, der dannes ved brug af topoisomerase-rettede kræftkemoterapeutika, haft den ulempe, at skaderne opstår sekvens-uspecifikt og overalt i arvemassen. Tidligere studier har derfor udelukkende anvendt genetiske mekanismer. Det cellulære Flp-nick system gør det muligt at kombinere genetike og molekylærbiologiske teknikker samt mikroskopi til at identificere reparationsfaktorer og nøje følge, hvad der sker ved kløvningsstedet, hvilke faktorer der rekrutteres til stedet, og hvor hurtigt reparationen sker.
Fremtidsperspektiver
Identificering af reparationsfaktorer vil muliggøre en evaluering af disse som nye mål i kræftkemoterapi. Stoffer målrettet mod disse reparationsfaktorer vil kunne anvendes i kombination med de eksisterende topoisomerase-rettede kemoterapeutika og øge bekæmpelsen af kræftcellerne og dermed effektiviteten af kræftkemoterapeutika.
Yderligere oplysninger
For yderligere oplysninger kontakt lektor Lotte Bjergbæk, Molekylærbiologisk Institut, Aarhus Universitet. E-mail: lbj@mb.au.dk, Tlf.: 8942 2702.
Den publicerede artikel: A Flp-nick system to study repair of a single protein-bound nick in vivo
Ida Nielsen1, Iben Bach Bentsen1, Michael Lisby2, Sabine Hansen1, Kamilla Mundbjerg1, Anni H Andersen1 & Lotte Bjergbaek1
1Department of Molecular Biology, University of Aarhus, Aarhus, Denmark.
2Department of Biology, University of Copenhagen, Copenhagen, Denmark.
