At holde cellekernen ren
Produktion af RNA i cell-kernerne i eukaryote organismer er under kontrol af det nukleære RNA-exosom hjulpet af adskillige co-faktorer. Forskere ved Aarhus Universitet og Københavns Universitet viser nu, hvordan to vigtige co-faktorer af det nukleære exosom genkender deres RNA-targets for at bevare en korrekt RNA-balance i cellekernen. Dette er vigtigt for cellernes – og dermed menneskers – overlevelse.
Celler er små fabrikker, der konstant producerer protein- og RNA-molekyler ved at afkode den genetiske information, der er gemt i kromosomernes DNA. Den første fase af denne afkodning, processen betegnet transskription, "transskriberer" DNA-koden til RNA-molekyler. Hos mennesker, og de fleste andre organismer, indeholder de fleste celler i kroppen organismens fulde genetiske information, selvom hver enkelt celle kun oplever en lille del af dens DNA blive afkodet. Alligevel er den første afkodningsfase (transskriptionen) ikke særligt specifik og dermed overproduceres en stor mængde RNA.
Disse overskydende RNA'er akkumulerer imidlertid ikke, idet de bliver nedbrudt kort efter deres syntese. Dette forhindrer akkumulering af ikke-funktionelle transskripter, der ellers ville være skadelige for normale cellulære funktioner. Det meste af denne nedbrydning udføres af det nukleære RNA-exosomkompleks, en RNA 3'-5 'exonuklease, som rekrutteres til RNA af dets specifikke adaptorer, såsom de såkaldte NEXT og PAXT komplekser.
Torben Heick Jensens laboratorium fandt tidligere, at NEXT og PAXT hjælper med til nedbrydning af forskellige slags nukleære RNA'er, men hvordan specificitet opnås, altså hvorledes de rigtige RNA’er bliver nedbrudt, var hidtil en gåde.
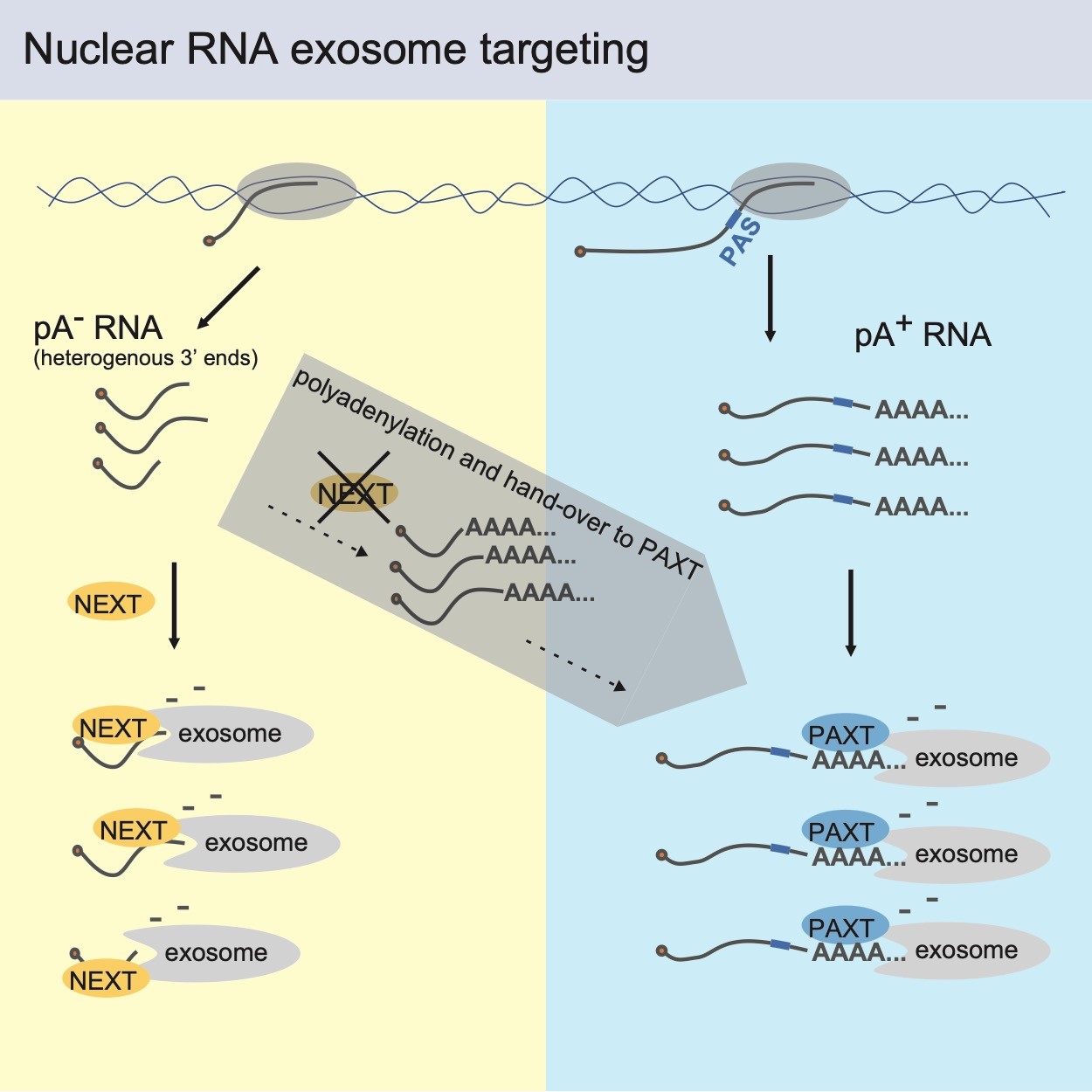
Forskerholdet offentliggør nu en videnskabelig artikel, hvor de afslører, at NEXT-substrater indeholder ’nøgne’ 3'ender, mens PAXT-substrater har 3'ender med såkaldte poly(A)-haler. På trods af denne klare substratopdeling afslørede studierne også, at disse to nedbrydningssystemer kan samarbejde, hvilket hjælper cellerne med at nedbryde NEXT-substraterne, selv i den potentielt farefulde situation, hvor NEXT-aktivitet er mindsket. I sådanne tilfælde får NEXT’s RNA-targets, der normalt er produceret uden en poly(A)-hale, tilføjet disse – et kendetegn ved PAXT-targets – hvilket udsætter dem for effektiv nedbrydning via PAXT-nedbrydningsvejen. Tilsammen giver dette en to-trins mekanisme, der sørger for en effektiv nukleær sortering af det humane transskriptom. Det næste store spørgsmål er nu, hvorledes disse RNA nedbrydningssystemer kobles til RNA produktion (transskription).
Disse fund er resultatet af et samarbejdsprojekt, der ledes af postdoc Guifen Wu og teamleder Manfred Schmid fra Torben Heick Jensen laboratorium ved Institut for Molekylærbiologi og Genetik, Aarhus Universitet, og i samarbejde med Leonor Rib og Albin Sandelin fra Biologisk Institut og Biotech Research and Innovation Centre (BRIC), Københavns Universitet. Undersøgelsen, der blev finansieret af Novo Nordisk Fonden og Lundbeckfonden, er offentliggjort i det internationale tidsskrift Cell Reports.
‘A two-layered targeting mechanism underlies nuclear RNA sorting by the human exosome’ by Guifen Wu, Manfred Schmid, Leonor Rib, Patrik Polak, Nicola Meola, Albin Sandelin, Torben Heick Jensen. Cell Reports.
Mere information
Postdoc Guifen Wu- wuguifen@mbg.au.dk
Teamleder Manfred Schmid- ms@mbg.au.dk
Professor Torben Heick Jensen - thj@mbg.au.dk – mobil: 60202705
Institut for Molekylærbiologi og Genetik, Aarhus Universitet
