Forskere fra Aarhus Universitet og Syddansk Universitet har opfundet en ny måde at kombinere liposomer med naturlige ekstracellulære vesikler. Det skaber et mere effektivt og mindre giftigt system til at levere mRNA end de traditionelle lipid-nanopartikler, som bruges i COVID-19-vacciner. Denne opdagelse åbner døren for fremskridt inden for naturlig medicinlevering.
Forskere fra Aarhus Universitet står bag en ny metode til at opdage vigtige proteiner i f.eks. en blodprøve. Ved hjælp af bittesmå nanoporer og nanobodies har de bl.a. identificeret markører, der er indikatorer for henholdsvis COVID-19 og brystkræft, med imponerende præcision og følsomhed. Med denne teknologi kan fremtiden byde på hurtig og præcis sygdomsdiagnose ved hjælp af en simpel blodprøve. Opdagelserne kan bringe os tættere på en forbedret sundhedspleje.
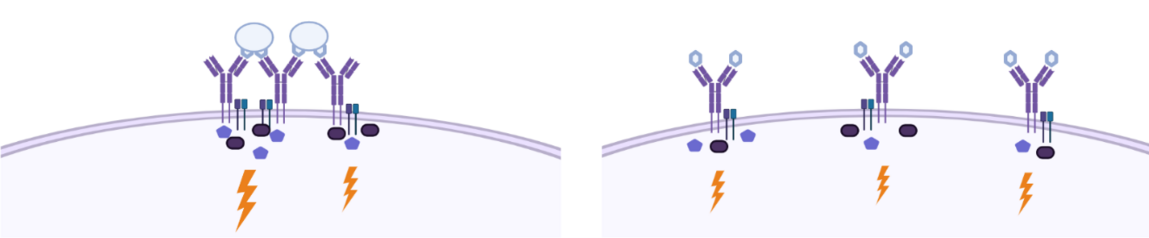
Forskere skaber et nybrud i forståelsen af, hvordan immunceller genkender trusler som fx virus. Opdagelsen kan bruges til at designe bedre vacciner og opnå en dybere indsigt i autoimmune sygdomme og allergier.
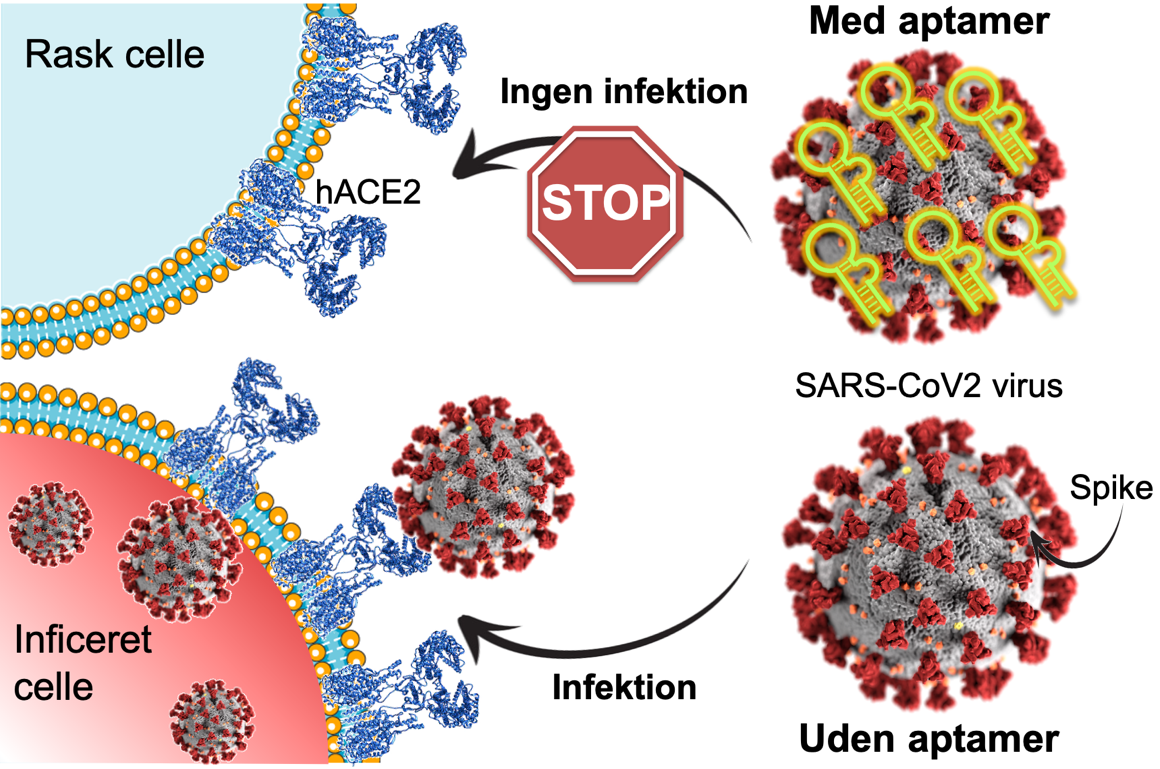
Et forskerhold fra Institut for Molekylærbiologi og Genetik og iNANO på Aarhus Universitet har brugt en in vitro selektionsteknik til at udvikle et RNA-molekyle, der genkender og binder Spike-proteinet fra coronaviruset SARS-CoV-2 med meget høj specificitet og styrke. Håbet er, at dette nye molekyle, også kaldet en aptamer, kan bidrage til bedre diagnostik og behandling af COVID-19 på længere sigt.
Jørgen Kjems' forskningsgruppe beskriver i en artikel i Nature Communications, hvordan de har udviklet en ny metode til at bestemme sekvensen af en klasse af RNA-molekyler kaldet cirkulært RNA (circRNA). Undersøgelser i hjerneprøver fra mennesker og mus viser, at circRNAer findes i mange forskellige versioner, og at en særlig klasse af genetiske elementer med en mulig rolle i autisme oftere findes i circRNA end i de mere hyppige lineære mRNAer.
Et såkaldt cirkulært RNA-molekyle, som man mente var kræftfremkaldende, findes alligevel i ikke i kræftceller. Et dansk forskerhold har offentliggjort de nye resultater i Nature Communications.
En ny artikel fra Jørgen Kjems' gruppe ved iNANO og MBG beskriver, hvordan mængden af det såkaldte 'ikke-kodende' RNA ændrer sig under epileptiske anfald. Forskerne fandt også ud af, at de ved at blokere specifikke molekyler kaldet mikroRNA'er kan mindske antallet af epileptiske anfald i en musemodel. Opdagelsen giver håb om, at disse RNA-molekyler kan tjene som mulige mål for fremtidig behandling af epilepsi.
Nye forskningsresultater med mus viser, at mængden af det såkaldte mikroRNA-128 har stor indflydelse på bevægeapparatet. Hvis niveauet af mikroRNA-128 hæves, giver det en lavere neuronaktivitet og kan derved være med til at hæmme de ukontrollerede bevægelser i forbindelse med epilepsi eller Parkinsons sygdom. Tilsvarende kan mikroRNA-128 sænkes for at øge neuronaktiviteten.
Et videnskabeligt samarbejde ledet af forskere ved iNANO/Institut for Molekylærbiologi og Genetik ved Aarhus Universitet og Kemisk Institut ved Københavns Universitet har ført til konstruktionen af en syntetisk DNA-nanopore, der er i stand til selektivt at translokere makromolekyler af proteinstørrelse på tværs af lipid-lag.
Danske og amerikanske forskere har fundet en hidtil ukendt underklasse af små RNA-molekyler, der er involveret i reguleringen af genekspression.
Et forskerhold ved Aarhus Universitet har karakteriseret en hidtil ukendt og revolutionerende måde celler kan regulere dannelsen af proteiner på. Dette involverer et overset cirkulært RNA-molekyle i menneskeceller samt et velkendt mikroRNA. Opdagelsen kan bidrage til en bedre forståelse for cellernes regulering af gener og dermed også for udvikling af kræft og andre sygdomme.
En forskergruppe fra Aarhus Universitet har sammen med forskere fra Australien og Norge fundet en ny, enkel og ikke-invasiv metode til at diagnosticere kræft i mundhulen på et tidligt stadium, hvilket er et af de vigtigste parametre for en vellykket behandling af kræft.
I et nyt forskningscenter drømmer man om at gøre en forskel for patienter med f.eks. diabetes, fedtlever, nyrefibrose og åreforkalkning. Med 60 millioner kr. fra Novo Nordisk Fonden kan centerleder Professor Jørgen Kjems nu åbne et tværfagligt center for RNA-medicinforskning ved Aarhus Universitet, som over en periode på 6 år vil udvikle mere effektive typer af behandling af stofskiftesygdomme.
Forskningsinitiativet LifeTime repræsenterer mere end 50 europæiske universiteter, herunder Aarhus Universitet. En ny Perspective-artikel i Nature, med Jørgen Kjems fra iNANO og MBG som medforfatter, skitserer LifeTimes vision om, hvordan man kan revolutionere sundhedsvæsenet gennem personlig, cellebaseret interceptiv medicin.
Professor Jørgen Kjems og konsortiet Virofight har modtaget støtte fra EU's FET-OPEN-program til fremme af ny antiviral behandling. I stedet for at ramme virusproteiner eller enzymer med små molekyler - som ved traditionelle antivirale midler - vil Virofight-projektet udvikle DNA-baserede nanoskaller, der kan indkapsle og neutralisere hele viruspartiklen. Denne nye strategi har potentialet til at kunne hjælpe med at bekæmpe et bredt udvalg af forskellige virustyper.
En af de store udfordringer i forbindelse med en genåbning af samfundet er adgangen til en hurtig og pålidelig test for SARS-CoV2-infektion. Med en bevilling fra Det Frie Forskningsråd vil Jørgen Kjems i samarbejde med forskere fra DTU og Rigshospitalet udvikle en metode, der kan påvise virussen i meget tidlige stadier af infektion og samtidig forudsige sværhedsgraden af kliniske symptomer patienten kan lide af.
Professor Jørgen Kjems fra MBG og iNANO skal i samarbejde med forskere fra Health, KU og Statens Serum Institut og med 25 mio. kr. fra Carlsbergfondet udvikle metoder til diagnostik, behandling og forebyggelse af SARS-CoV-2-infektioner. Målet er samtidig at ruste verden til bedre at kunne modstå fremtidige virusepidemier.
Jørgen Kjems, professor ved Institut for Molekylærbiologi og Genetik og iNANO, modtager Novo Nordisk Prisen 2018 for sine tværfaglige pionerstudier af, hvordan DNA’s biologiske fætter, RNA, spiller en helt central rolle i cellers regulering og har et kæmpe potentiale i fremtidens sygdomsbehandling.
Potentialet er enormt for den forskning, som Center for Multifunctional Biomolecular Drug Design (CEMBID) på Aarhus Universitet nu tager fat på. Målet er at skabe en ny generation af lægemidler, som kan bruges til at diagnosticere og behandle kræft og åreforkalkning – som tilsammen udgør to tredjedele af dødsårsagerne globalt.
Et nyt grundforskningscenter, CellPAT, skal afdække, hvordan celler taler med hinanden og dermed gøre det muligt at forebygge eller rette den slags fejlkommunikation, som gør os syge.
Carlsbergfonden har tildelt Jørgen Kjems 6,1 mio. kr. til at udvikle en helt ny metode, der kan “oversætte” det samlede indhold i en fødevare til digitaliseret information i form af DNA-sekvenser.
Professor Jørgen Kjems er blevet udnævt til centerleder på iNANO for en tre-årig periode. Jørgen Kjems har været en integreret del af ledelsen på centret gennem flere år. Han var i sin tid med til at grundlægge iNANO og har været konstitueret som leder i 2014.
Et nydannet konsortium, der involverer 16 partnere fra 8 europæiske lande, USA og Brasilien har modtaget 11,5 mio. Euro i støtte fra Den Europæiske Unions 7. Rammeprogram til at undersøge molekylære mekanismer, diagnostik og behandling af epilepsi. Jørgen Kjems fra Institut for Molekylærbiologi og Genetik/iNANO er leder af den århusianske del af konsortiet.
Jørgen Kjems og Ken Howard modtager en treårig bevilling på 9.8 mio. kr. fra Det Strategiske Forskningsråd til et projekt til udvikling af nye lægemidler mod cystisk fibrose og tarmsygdomme, der skyldes betændelse.